1������� ����������������������ע����Һ���ش��������⣮
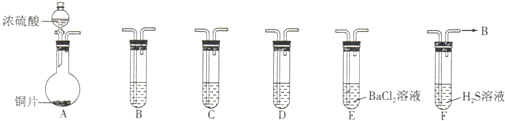
��1������װ��A��д��ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ��______����ƿ�е�ʵ������Ϊ______��
��2����֤̼����ǽ����Ե����ǿ������֪���ԣ�H2SO3��H2CO3������ѡ������A��B��C��D�������ӣ���B��C��D����ѡ����Լ��ֱ�Ϊ______��______��______����˵��̼�ķǽ����Աȹ�ǿ��ʵ��������______��
��3����֤SO2�������ԡ���ԭ�ԣ���ѡ��A��E��F����������A��E��F˳�����ӣ�
����֤��SO2�������Ե�ʵ��������______����Ӧ����ʽΪ��______��
����֤��SO2���л�ԭ�ԣ���E�в�ȡ��ʵ�����Ϊ______����ʵ������Ϊ______����Ӧԭ��Ϊ______��
�ο��𰸣���1��ͭ��Ũ���ᷴӦ��ͭ���л�ԭ�ԣ�Ũ�������ǿ�����ԣ���Ӧ������Ȳ��ܷ�������д��ѧ����ʽΪ��Cu+2H2SO4��Ũ����.CuSO4+2H2O+SO2������������������������ɣ�����ͭ����������ð��������Ũ������������ԣ�����������ͭ���ɣ�ͭƬ���ɫ��Ũ���������ˮ�ԣ����ɵ���ˮ����ͭ�ʰ�ɫ���ʴ�Ϊ��Cu+2H2SO4��Ũ����.CuSO4+2H2O+SO2����ͭƬ��Һ�ɫ�������������ɣ���ƿ�п����а�ɫ�������ɣ�
��2��װ��A�������dz�ȥ��������װ��B�������Dz���������̼������̼���ƻ�̼�����ƣ�װ��C�������dz�ȥ��������������ǿ�����������磺���Ը��������Һ���ɷ�ֹ���Ŷ�����̼���������Һ�ķ�Ӧ��װ��D��������֤��̼�����Աȹ���ǿ��ѡ������Թ����Σ����������Һ������ǿ���Ʊ����ᣬ����Խǿ�����������ˮ���������Խǿ������Ԫ�صķǽ�����Խǿԭ�����ʿ���������ΪC��KMnO4��Һ����ɫ��D�г��ְ�ɫ������
�ʴ�Ϊ��Na2CO3��Һ�� NaHCO3��Һ��KMnO4 ��Һ��Na2SiO3��Һ��C��KMnO4��Һ����ɫ��D�г��ְ�ɫ������
��3����H2S��Һ�ж������������ⷴӦ����������ˮ����������Ļ��ϼ۽�����Ϊ�����������������ԣ����Կ�������ɫ���dz��֣�
��Ӧ���ӷ���ʽΪ��2H2S+SO2=3S��+2H2O��
�ʴ�Ϊ��H2S��Һ����dz��ɫ���dz��֣� 2H2S+SO2�T3S��+2H2O��
��Ҫ֤������������л�ԭ�ԣ��ɰѶ����������������ᣬͨ�����������������֤�����ʿɰѶ�������ͨ���Ȼ�����Һ�в���Ӧ���μ���ˮ�������ػ����������������Ѷ����������������ᣬ�������Ȼ�����Ӧ�������ᱵ���漰����ʽΪBa2++SO2+Cl2+2H2O=BaSO4��+4H++2Cl-��
�ʴ�Ϊ��ͨ���������������ˮ��������������Һ������������Һ��������������ɫ�������ɣ�Ba2++SO2+Cl2+2H2O=BaSO4��+4H++2Cl-��
���������
�����Ѷȣ�һ��
2��ѡ���� ����ʵ���ܴﵽԤ��Ŀ���ǣ�������
| ��� | ʵ����� | ʵ��Ŀ��
A
����ϩ������Ļ������ͨ�����Ը��������Һ
��ȥ�����л��е���������ϩ
B
��������м��뱥��̼������Һ����Һ
��ȥ���������л��е�����������
C
����ˮ�м���ƾ�����Һ
��ȡ��ˮ�еĵ�
D
ȡ��������ˮ�⣨ˮ��ʱ�������������������Һ���������Ƶ�Cu��OH��2����Һ������
������۵�ˮ�����
|