1、选择题 最近,科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰.电池总反应为:Zn+2MnO2+H2O=ZnO+2MnO(OH).下列说法正确的是( )
A.该电池Zn为负极,ZnO为正极,MnO2为催化剂
B.该电池的负极反应为:MnO2+e-+H2O=MnO(OH)+OH-
C.导电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn
D.电池工作时水分子和OH-都能通过薄层纸片
参考答案:A、从电池反应可知,锌失去电子被氧化,所以是负极,MnO2为正极,故A错误;
B、该电池反应中锌失去电子被氧化,所以是负极,电极反应为Zn-2e-+2OH-=ZnO+H2O,故B错误;
C、导电时外电路电子由负极经外电路流向正极,即Zn流向MnO2,内电路是离子的定向移动形成电流,故C错误;
D、“软电池”采用薄层纸片作为载体和传导体,电池工作时水分子和OH-都能通过薄层纸片,故D正确.
故选D.
本题解析:
本题难度:简单
2、实验题 (15分)高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂。电解法制备高铁酸钾操作简便,成功率高,易于实验室制备。其原理如下图所示。
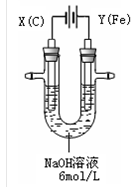
I. 实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。
(1)电解过程中,X极是 极,电极反应是 。
(2)电解过程中,Y极放电的有 。
(3)生成高铁酸根(FeO42-)的电极反应是 。
II. 若用不同种电池作为上述实验的电源,请分析电池反应。
(1)铅蓄电池总的化学方程式为:
2H2O+2PbSO4 Pb+PbO2+2H2SO4,则它在充电时的阳极反应为
Pb+PbO2+2H2SO4,则它在充电时的阳极反应为
。
(2)镍镉碱性充电电池在放电时,其两极的电极反应如下:
正极:2NiOOH+2H2O+2e-=2Ni(OH)2+2OH-
负极:Cd+2OH--2e-=Cd(OH)2
则它在放电时的总反应的化学方程式为 。
(3)肼(N2H4)是一种可燃性液体,可用作火箭燃料。已知在25℃、101kPa时,32.0g N2H4在氧气中完全燃烧生成氮气和液态水,放出624kJ的热量,则N2H4完全燃烧的热化学方程式是 ;
肼―空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液,放电时负极的电极反应是 。
(4)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐,电池总反应方程式为:C3H8+5O2=3CO2+4H2O。
写出该电池正极的电极反应: 。
(5)当制备相同物质的量的高铁酸钾时,理论上,上述四种电池中分别消耗的Pb、Cd、肼、丙烷的物质的量之比是 。
参考答案:Ⅰ.(1)阴;2H++2e-= H2↑。(2)Fe和OH- (3)Fe+8OH--6e-= FeO42-+4H2O
Ⅱ.(1)PbSO4+2H2O-2e-= PbO2+SO42-+4H+
(2)Cd+2NiOOH+2H2O = Cd(OH)2+2Ni(OH)2
(3)N2H4(1)+O2(g)= N2(g)+2H2O(l)△H=-624kJ/mol
N2H4+4OH--4e-= 4H2O+N2↑
(4)O2+2CO2+4e-= 2CO32-
(5)10:10:5:1
本题解析:I.(1)X和电源的负极相连,所以是阴极,溶液中的氢离子放电,方程式为2H++2e-= H2↑。
(2)Y和电源的正极相连,作阳极。由于Y是铁,所以铁失去电子,发生氧化反应。根据实验现象可判断,在阳极上溶液中的OH-也放电生成氧气。
(3)阳极铁失去电子,氧化产物是高铁酸根,反应式为Fe+8OH--6e-= FeO42-+4H2O。
II.(1)充电相当于电解,在电解池中阳极失去电子,发生氧化反应。根据反应式可判断,充电时硫酸铅失去电子,所以电极反应式为PbSO4+2H2O-2e-= PbO2+SO42-+4H+。
(2)在原电池中正负极的电极反应式相叠加即得到总反应式,所以反应式为Cd+2NiOOH+2H2O = Cd(OH)2+2Ni(OH)2。
(3)32.0g N2H4是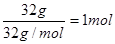 ,所以热化学方程式为N2H4(1)+O2(g)= N2(g)+2H2O(l)△H=-624kJ/mol。在燃料电池中负极是失去电子的,所以肼在负极通入,发生氧化反应,氧化产物是氮气,反应式为N2H4+4OH--4e-= 4H2O+N2↑。
,所以热化学方程式为N2H4(1)+O2(g)= N2(g)+2H2O(l)△H=-624kJ/mol。在燃料电池中负极是失去电子的,所以肼在负极通入,发生氧化反应,氧化产物是氮气,反应式为N2H4+4OH--4e-= 4H2O+N2↑。
(4)负极通入丙烷,丙烷的氧化产物是CO2和水,由于电解质水熔融的碳酸盐,所以电极反应式为C3H8-20e-+10CO32-=13CO2+4H2O,根据总反应式可知,正极反应式为5O2+10CO2+20e-= 10CO32-。
(5)1molPb、Cd、肼、丙烷失去的电子分别为2mol、2mol、4mol、20mol,所以根据得失电子守恒可知,Pb、Cd、肼、丙烷的物质的量之比是10:10:5:1。
本题难度:困难
3、选择题 Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4―SOCl2。电池的总反应可表示为:4Li+2SOCl2 =" 4LiCl" +S +SO2。下列说法中不正确的是
A.该电池的负极反应为2SOCl2 + 4e― = S +SO2+4Cl―
B.该电池的负极反应为4Li = 4Li+ + 4e―
C.反应SOCl2 + H2O = SO2↑ + 2HCl↑为非氧化还原反应
D.组装该电池必须在无水的条件下进行
参考答案:A
本题解析:A、负极发生氧化反应,为4Li-4e-=4Li+,错误;B正确;
C、没有化合价的改变,为非氧化还原反应。
D、因为SOCl2与水发生水解反应,故在无水条件下进行。
本题难度:困难
4、选择题 铅蓄可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:
2PbSO4+2H2O  ?Pb+PbO2+2H2SO4,下列判断不正确的是(?)
?Pb+PbO2+2H2SO4,下列判断不正确的是(?)
A.其充电过程作为电解池,放电过程作为原电池
B.充电时,PbSO4在阴极转化为PbO2
C.放电时,Pb作为负极
D.放电时,PbO2发生还原反应
参考答案:B
本题解析:铅蓄电池中放电相当于原电池,充电相当于电解池,A正确。根据反应式可知,充电时阴极是得到电子的,所以PbSO4在阴极转化为Pb,B不正确。原电池中负极失去电子,发生氧化反应。正极得到电子,发生还原反应,因此选项CD都是正确的,答案选B。
本题难度:简单
5、选择题 用铅蓄电池电解苦卤水 (含C1-、Br-、Na+、Mg2+)的装置如图所示 (a、b为石墨电极)。下列说法中正确的是(?)
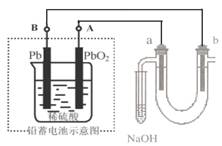
A.铅蓄电池负极的反应式为:Pb → Pb2++ 2e -
B.铅蓄电池放电时,该电池两极质量均减少
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a 电极首先放电的是Br-
参考答案:D
本题解析:略
本题难度:一般