1������� ��ҵ����ij����������Cu2O��Al2O3��Fe2O3��SiO2����ȡͭ�IJ����������£���������E������ҺC��ȡ����

��֪��Cu2O + 2H+?=" Cu" + Cu2+ + H2O��
��1����ҺA����Ԫ�صĿ��ܴ�����ʽΪ_______�������ӷ��ţ�����֮��ص����ӷ���ʽΪ_____________������ҺA�д���Fe3+����������ӵ��Լ�Ϊ________�����Լ����ƣ���
��2��д��E��F��Ӧ����ͭ�Ļ�ѧ����ʽΪ_____________________________��
��3�����õ�ⷨ���д�ͭ����ʱ������������ȷ����_________������ţ���
a����������ͭ��Һ�����Һ��SO2- 4�������ƶ�
b����ͭ�ӵ�Դ������������ԭ��Ӧ
c����ͭ��������������Һ��Cu2+Ũ�ȼ�С
d������ͭ����6.4 gʱ��ת��0.2NA������
�ο��𰸣�(12��)
Fe2+��Fe2+��Fe3+��2�֣���Fe2O3+6H+="2" Fe3++3H2O��2�֣���2Fe3++Cu=2Fe2++ Cu2+��2�֣���
���軯����Һ������������ͬ�����֣���2�֣�
(2)? 2Al+3CuO= Al2O3+3Cu��2�֣�
(3)? c��2�֣�
���������Fe2O3��Al2O3��CuO��SiO2��SiO2�������Ӧ��Fe2O3��Al2O3��Cu2O��Ӧ��Cu2O + 2H+?=" Cu" + Cu2+ + H2O��Fe2O3+6H+="2" Fe3++3H2O��Al2O3+6H+=2 Al3++3H2O����2Fe3++Cu=2Fe2++ Cu2+���ɷ�������ҺA�е�����һ����H+��Cu2+��Al3+��������Fe2+��ͭ�϶ࣩ��Fe2+��Fe3+��ͭ���٣����ټ�������NaOH���ɹ���Cu(OH)2�����������������������ת��ΪF(Fe2O3��CuO�Ļ����)����ҺCΪƫ�����ƺ�NaOH�Ļ��Һ������ȡ����E(ΪAl�ĵ���)��
��1��������Fe2+��Cu2O�϶ࣩ��Fe2+��Fe3+��Cu2O���٣���
��2�����ȷ�Ӧ2Al+3CuO= Al2O3+3Cu��
��3����ⷨ���д�ͭ����ʱa��SO2- 4�������ƶ�������b����ͭ�ӵ�Դ����������������Ӧ��������������c����ͭ����������������ͭ�����ʽ����ŵ磬����ֻ��Cu2+�ŵ磬���Ե�����Һ��Cu2+Ũ�ȼ�С����ȷ��d������ͭ����6.4 gʱ����������ͭ�����ʽ����ŵ磬ʧȥ���Ӳ�һ��Ϊ0.2NA��������
�����Ѷȣ�һ��
2������� (10��)��ѧԭ����Ӧ���ڹ�ҵ���������ȼҵ�����Ṥҵ��
��1���ȼҵ�õ����豸Ϊ���ӽ���Ĥ���ۣ����ʱ��������? ___________(���Լ�����)����������Ϊ_________________���ѧʽ��,�����ܷ�Ӧ����ʽ____________________________________________________.
��2���Ӵ�����������Ҫ�ֳ���������һ�������ջ�������___________�н��У��ڶ����Ǵ�������������Ӧ�ķ���ʽ___________________________________________,
��������������������ȡ�Ʊ�������������1mol/L����������Һ�к�,��������������Һ�����Ϊ400mL���ų�����ΪQ kJ,д����ʾ�÷�Ӧ�к��ȵ��Ȼ�ѧ����ʽ___________________________________________________��
�ο��𰸣���1������ʳ��ˮ��1�֣�? H2 NaOH ��2�֣�ȱһ���ɣ�
2NaCl? +? 2H2O ="=" 2NaOH + H2��+Cl2��(�������)��2�֣�
��2������¯��1�֣�? 2SO2+ O2 2SO3 (������������) 2��
2SO3 (������������) 2��
NaOH(aq)��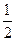 H2SO4(aq)===
H2SO4(aq)===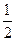 Na2SO4(aq)��H2O(l)����H����2.5Q kJ��mol��1
Na2SO4(aq)��H2O(l)����H����2.5Q kJ��mol��1
�����������
�����Ѷȣ���
3������� �±��г���3��ȼú����������ԭ����
������
| �ð�ˮ��SO2ת��ΪNH4HSO3����������(NH4)2SO4
|
������
| ���������Ƚ���(��Ҫ�ɷ�CO��CH4��H2)��SO2�ڸ����»�ԭ�ɵ�����
|
������
| ��Na2SO3��Һ����SO2���پ����ת��ΪH2SO4
|
?
(1)�������а�ˮ����ȼú������SO2�Ļ�ѧ��ӦΪ��
2NH3��SO2��H2O=(NH4)2SO3
(NH4)2SO3��SO2��H2O=2NH4HSO3
�����ȼú������SO2ȥ���ʵĴ�ʩ��________(����ĸ)��
A������ˮŨ��
B�����߷�Ӧ�¶�
C��ʹȼú�����백ˮ��ֽӴ�
D��ͨ�����ʹHSO3-ת��ΪSO42-
���÷�������������ҪԤ�ȳ�ȥȼú�����д�����CO2��ԭ����____________(�����ӷ���ʽ��ʾ)��
(2)����������Ҫ���������з�Ӧ��
2CO(g)��SO2(g)=S(g)��2CO2(g)����H��8.0 kJ��mol��1
2H2(g)��SO2(g)=S(g)��2H2O(g)����H��90.4 kJ��mol��1
2CO(g)��O2(g)=2CO2(g)����H����566.0 kJ��mol��1
2H2(g)��O2(g)=2H2O(g)����H����483.6 kJ��mol��1
S(g)��O2(g)��Ӧ����SO2(g)���Ȼ�ѧ����ʽ�ɱ�ʾΪ________��
(3)���������ö��Ե缫���NaHSO3��Һ��װ������ͼ��ʾ���������ų�����ijɷ�Ϊ________(�ѧʽ)��
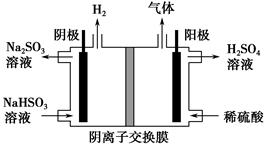
�ο��𰸣�(1)AC��HCO3-��SO2=CO2��HSO3-
(2)S(g)��O2(g)=SO2(g)��H����574.0 kJ��mol��1
(3)O2��SO2
���������(1)����ˮŨ�ȣ��ܷ�Ӧ���϶��SO2�������SO2ȥ���ʣ����߷�Ӧ�¶�ֻ�ܼӿ컯ѧ��Ӧ���ʣ���(NH4)2SO3��NH4HSO3�����ֽ⣬������SO2����SO2ת��ΪNH4HSO3ʱ��ͨ��Ŀ������ܽ�����������������ֱ������SO2�����Բ������SO2ȥ���ʡ�
(2)���ݸ�˹���ɣ�Ӧ�÷��̢٣����̢۵õ�
SO2(g)=S(g)��O2(g)����H��8.0 kJ��mol��1��(��566.0 kJ��mol��1)��574.0 kJ��mol��1����S(g)��O2(g)=SO2(g)����H����574.0 kJ��mol��1��Ҳ���÷��̢ܣ����̢���á�
(3)���ݵ��ԭ����NaHSO3��Һ�е�����������������������Ӧ����4OH����4e��=2H2O��O2����������������ͨ��ϡ���ᣬH����HSO3-=H2O��SO2��������������������ΪO2��SO2��
�����Ѷȣ�һ��
4������� ����ѧ--ѡ��2��ѧ�뼼������15�֣�
������أ�K2FeO4����һ�ּ�������������������һ������Ͷ��ˮ���������������������£�
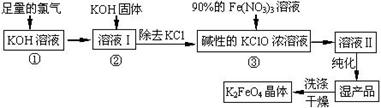
��֪��2KOH + Cl2 �T KCl + KClO + H2O���������¶Ƚϵͣ�
����? 6KOH + 3Cl2 �T 5KCl + KClO3 + 3H2O���������¶Ƚϸߣ�
�����ش��������⣺
��1�����������շ�Ӧ��Ӧ�������� ����¶Ƚϸߡ����¶Ƚϵ͡���������½��У�
��2��д����ҵ����ȡCl2�Ļ�ѧ����ʽ�������������� ����������������������
��3��K2FeO4����ǿ�����Ե�ԭ������������������������ ��
��4������KOH��Һʱ������ÿ100 mLˮ���ܽ�61.6 g KOH���壨 ����Һ���ܶ�Ϊ1.47 g/mL������
�����ʵ���Ũ��Ϊ������ ��������������������������
��5���ڡ���ҺI���м�KOH�����Ŀ������������ ������������������������
A���� ����ҺI�� �й�����Cl2������Ӧ�����ɸ����KClO
B��KOH�����ܽ�ʱ��ų��϶����������������߷�Ӧ����
C��Ϊ��һ����Ӧ�ṩ��Ӧ�����
D��ʹ������KClO3ת��Ϊ KClO