1��ѡ���� 46g�������ڿ����г��ȼ�յõ�����ɫ��ĩ���÷�ĩ��������ˮ��Ӧ�ų����������ǣ���״����)
A.44.8L
B.11.2L
C.22.4L
D.5.6L
�ο��𰸣�B
���������46g����2mol������1mol Na2O2���������ƺ�ˮ��Ӧ����0.5mol��������״���µ������11.2L����ѡB��
�����Ѷȣ�һ��
2��ѡ���� ij������Ļ�ѧʽΪC4H9Cl�����Ŀ��ܵĽṹ�м���
A.2
B.3
C.4
D.5
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3��ѡ���� �������и������ӵ���Һ�У�ͨ�루����룩������ij�����ʺ����ܴ����������
A.H+��Ba2+��Fe3+��NO3�D��ͨ��SO2����
B.Ca2+��Cl�D��K+��H+��ͨ��CO2����
C.Al(OH)4-��Na+��Br-��SO42-��ͨ��CO2����
D.HCO3����Na+��I�D��HS�D������AlCl3��Һ
�ο��𰸣�B
���������A��ͨ������������巢��������ԭ��Ӧ��2H2O+ 2NO3�D+ 3SO2= 3SO42-+2NO��+4H+��2H2O+2Fe3++SO2=2Fe2++ SO42-+4H+�����ɵ�SO42-��Ba2+�γɳ�����A����C��ͨ����������̼���巢����ӦAl(OH)4-+ CO2=Al(OH)3��+HCO3-�����Ӳ��ܴ������棬C����D�м�������Ȼ�����Һ������Ӧ3HCO3��+Al3+= Al(OH)3��+3CO2����Al3++ 3HS�D+3H2O= Al(OH)3��+3H2S�������Ӳ��ܴ������档
���㣺���ӹ���
�����������������ǿ��ԭ�ԣ�������������������Fe3+��HNO3�����Ը��������Һ��˫��ˮ�ȣ���Ӧ��
�����Ѷȣ���
4������� �ڣ�Te��Ϊ��A��Ԫ�أ��ǵ�����¼����²��ϵ���Ҫ�ɷ�֮һ����ҵ�Ͽɴӵ�⾫��ͭ������������ȡ�ڡ�
��1����ͭ�к���Cu������Zn��Ag��Au��TeO2�������������⾫��������������Ҫ����TeO2�������������ʼ������������⾫����ͭʱ�������缫��ӦʽΪ ��
��2��TeO2���������������ˮ��������ǿ���ǿ�����������������ȡ�ڵ�һ�ֹ����������£�
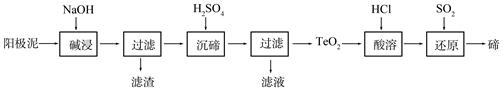
�١������ʱTeO2������Ӧ�Ļ�ѧ����ʽΪ ��
�ڡ����ڡ�ʱ������Һ��pHΪ4.5-5.0������TeO2���������H2SO4��������Һ��ȹ��������ڵij�������ȫ��ԭ���� ����ֹ�ֲ���ȹ���IJ��������� ��
�ۡ����ܡ���SO2ͨ��TeCl4��Һ�н��С���ԭ���õ��ڣ��÷�Ӧ�Ļ�ѧ����ʽ�� &# 160; ��
�ο��𰸣���1��Zn-2e-=Zn2+ Cu-2e-=Cu2+ ����4�֣���2�֣�
��2���� TeO2+2NaOH=Na2TeO3+H2O ��3�֣�
��TeO2�����������H2SO4�����ᵼ��TeO2������H2SO4��Ӧ������ʧ����3�֣�
��������H2SO4�������Ͻ��� ��3�֣�
�� TeCl4 + 2SO2 + 4H2O="Te" + 4HCl + 2H2SO4 ��3�֣�
�����������1����⾫����ͭʱ����ͭ�е�Cu������Zn����������������Ӧ��Zn��Cu���ã���ʧ���ӣ����������缫��ӦʽΪZn-2e-=Zn2+ Cu-2e-=Cu2+
��2����TeO2��������������������Ʒ����������������������Ƶķ�Ӧ����ѧ����ʽΪTeO2+2NaOH=Na2TeO3+H2O��
����ΪTeO2�����������H2SO4�����ᵼ��TeO2������H2SO4��Ӧ������ʧ����ֹ�ֲ���ȹ���IJ��������ǻ�������H2SO4�������Ͻ��裻
��SO2��ԭTeCl4ΪTe������������Ϊ���ᣬ��ѧ����ʽΪTeCl4+2SO2+4H2O=Te+4HCl+2H2SO4
���㣺�����ͭ�����ĵ�ⷴӦʽ����д���Ը��������Ļ�ѧ����ʽ���жϼ���д��ʵ��������ж�
�����Ѷȣ�����
5��ѡ���� �����������ʲ�����ͬ���칹�����
A.������ ?����
B.���� ?��ѿ��
C.������ ?�춡��
D.���� ?����
�ο��𰸣�D
���������D�����ۺ���ά����Ȼ��ѧʽ��ͬ�����ۺ϶Ȳ�ͬ���ϸ������Ͻ�����ѧʽ��ͬ�����ܳ���ͬ���칹��
�����Ѷȣ�����