1、选择题 某溶液中大量存在以下五种离子: Cl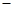 、SO42-、Fe3+、H+、M,其物质的量浓度之比
、SO42-、Fe3+、H+、M,其物质的量浓度之比
为c(Cl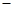 )︰c(SO42—)︰c(Fe3+)︰c(H
)︰c(SO42—)︰c(Fe3+)︰c(H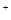 )︰c(M)=5︰3︰2︰3︰2,则M可能是(? )
)︰c(M)=5︰3︰2︰3︰2,则M可能是(? )
A.Ag+
B.Mg2+
C.NO
D.Na+
参考答案:D
本题解析:根据溶液中正电荷总数+负电荷总数="0"
5×Cl-+3×SO42- =2×Fe3++3×H++2×M
5+6=6+3+2M
M=1
即,M为+1价的阳离子选项中,AD符合但,Ag+和Cl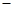 会结合生成AgCl、无法大量共存。所以,唯一符合要求的是Na+故选D
会结合生成AgCl、无法大量共存。所以,唯一符合要求的是Na+故选D
本题难度:一般
2、选择题 下列离子方程式书写正确的是(?)
A.碳酸钙溶于醋酸:CaCO3+2H+=Ca2++H2O+CO2↑
B.向NaHCO3溶液中滴加AlCl3溶液:Al3++3HCO3-=Al(OH)3↓ + 3CO2↑
C.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-= CO32-+H2O
D.SO2气体通人Ba(NO3)2溶液中:SO2+H2O+Ba2+=BaSO3↓+2H+
参考答案:B
本题解析:A项:醋酸是弱电解质,应写成化学式,故错。C项:少些了一个反应,故错。D项:因为HNO3具有强氧化性,沉淀生成的应为BaSO4,故错。故选B。
点评:离子方程式正误判断要注意:看原则:看是否符合客观事实、看是否符合质量守恒、看是否符合电荷守恒、看是否符合得失电子相等。可溶的易电离的物质拆成离子。注意过量、少量、适量等。
本题难度:简单
3、选择题 在溶液中能够大量共存的离子组是
A.Ca2+、Cl-、CO32-、Na+
B.Cl-、CO32-、Na+ 、H+
C.H+、Ba2+、OH-、NO3-
D.Mg2+、Na+、Cl-、SO42-
参考答案:D
本题解析:A、Ca2+与CO32-可生成沉淀
B、CO32-与H+不能大量共存
C、H+与OH-将生成水
D、正确
本题难度:一般
4、选择题 在下列各溶液中,离子一定能大量共存的是(?)
A.强酸性溶液中:Na+、、Mg3+、Cl-、AlO2-
B.含有0.5 mol·L-1 Al3+的溶液中:K+、Cl-、CO32-、NO-3
C.含有0.5 mol·L-1 Ca2+的溶液中:Na+、K+、HCO3-、Cl-
D.室温下,pH=13的溶液中:Na+、K3+、NO-3、HCO3-
参考答案:C
本题解析:略
本题难度:一般
5、选择题 在由水电离产生的c(H+)?=?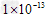 mol/L的溶液中,一定能大量共存的离子组是
mol/L的溶液中,一定能大量共存的离子组是
[? ]
A.K+、Cl-、NO3-、HCO3-
B.K+、Fe2+、I-、NO3-
C.Na+、Cl-、NO3-、SO42-
D.Al3+、AlO2-、Cl-、HS-
参考答案:C
本题解析:
本题难度:一般