1、选择题 液态CS2能够在O2中燃烧生成CO2和SO2两种气体,今用0.228 g CS2在448 mL氧气(标准状况)中完全燃烧,反应后混合气体在标准状况下体积为()
A.112 Ml
B.224 mL
C.336 mL
D.448 mL
参考答案:D
本题解析:根据反应前后元素原子个数守恒的规律,可得化学方程式:CS2+3O2 CO2+2SO2,分析方程式可知这是一个反应前后气体的物质的量不变的反应,因而在同温同压下气体的体积也不变。
CO2+2SO2,分析方程式可知这是一个反应前后气体的物质的量不变的反应,因而在同温同压下气体的体积也不变。
本题难度:简单
2、选择题 下列各组物质中,所含分子数相同的是
[? ]
A.?10g?H2和10g?O2?
B.?5.6?LN2(在标准状况下)和10g?CO2?
C.?9g?H2O?和0.5?mol?Br2?
D.?224?mL?H2?(在标准状况下)和0.1?mol?N2
参考答案:C
本题解析:
本题难度:简单
3、选择题 设NA为阿伏加德罗常数的数值,下列说法正确的是(?)。
A.常温下,4 g CH4含有NA个C―H共价键
B.1 mol Fe 与足量的稀HNO3反应,转移2NA个电子
C.1 L 0.1 mol・L-1 NaHCO3溶液中含有0.1NA个HCO3-
D.常温常压下,22.4 L的NO2和CO2混合气体含有2NA个O原子
参考答案:A
本题解析:由1 mol CH4中含有4 mol C―H共价键,4 g CH4的物质的量为0.25 mol,含0.25 mol×4×NA mol-1=NA个C―H共价键,A正确;1 mol Fe被足量的稀HNO3氧化成Fe3+,转移3NA个电子,B不正确;HCO3-既能水解又能电离,C不正确;常温常压下,22.4 L的NO2和CO2混合气体物质的量小于1 mol,则含有O原子数目小于2NA个,标准状况下22.4 L该混合气体含有O原子数目才为2NA个,D不正确。
本题难度:一般
4、计算题 将3.25g锌投入200mL某浓度的盐酸中,锌和盐酸恰好完全反应。
求:(1)反应中生成的H2在标准状况下的体积;
(2)所用盐酸中HCl的物质的量浓度。
参考答案:1.12L;0.5mol/L
本题解析:n(Zn)=3.25g÷65g/mol=0.05mol,则根据反应式可知
Zn + 2HCl ="=" ZnCl2 + H2↑
1 mol 2 mol 1 mol
0.05mol 0.1mol 0.05mol
所以V(H2)=0.05mol ×22.4L/mol ="=" 1.12L
c(HCl)= 0.1mol÷0.2L=0.5mol /L
考点:考查物质的量的有关计算
本题难度:一般
5、选择题 设NA表示阿伏加德罗常数值,下列叙述正确的是
A.54g H218O中含有电子总数为30NA个
B.11.2L H2中含有的电子数为NA个
C.23gNa+含有的最外层电子数为NA个
D.16g氧气和16g臭氧含有的核外电子总数均为8NA
参考答案:D
本题解析:A:H218O中含有电子数为10个,式量为20,则54g H218O中含有电子总数为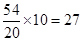 NA个;B:只说明气体的体积,不表明状态是没有意义的;C:Na+的最外层电子数为8,所以23gNa+含有的最外层电子数为8NA个;D:氧气和臭氧均是由氧原子组成的,16g含有1mol氧原子,含有的核外电子总数均为8NA,故答案为D
NA个;B:只说明气体的体积,不表明状态是没有意义的;C:Na+的最外层电子数为8,所以23gNa+含有的最外层电子数为8NA个;D:氧气和臭氧均是由氧原子组成的,16g含有1mol氧原子,含有的核外电子总数均为8NA,故答案为D
本题难度:一般