1、选择题 下列各组物质中,前者为附着在容器内壁的污物,后者能溶解前者的是(?)
①银镜――硝酸? ②水垢――醋酸? ③硫磺――二硫化碳? ④苯酚――酒精
⑤硝基苯――乙醚? ⑥油脂――浓热的碳酸钠溶液
A.只有①②③
B.只有①④⑥
C.只有②③⑤
D.全部
参考答案:D
本题解析:硝酸是氧化性酸,能溶解银。水垢的主要成份是碳酸钙和氢氧化镁,均能溶解在醋酸中。硫易溶在二硫化碳中。苯酚易溶在酒精中,硝基苯能溶解在有机溶剂乙醚中。热的碳酸钠溶液碱性比较强,能使油脂水解。所以正确的答案是D。
本题难度:一般
2、选择题 在进行下列实验时,采取的安全防护措施错误的是(?)
A.蒸发结晶时,用玻璃棒不断搅拌溶液
B.进行蒸馏操作时,先在蒸馏烧瓶中加入几块沸石
C.给试管中的液体加热时,先预热,再对准液体中下部加热
D.稀释浓硫酸时,将水沿烧杯壁慢慢倒入浓硫酸中,并不断搅拌
参考答案:D
本题解析:略
本题难度:简单
3、选择题 下列实验操作所用仪器合理的是( )
A.将CCl4与溴水混合后振荡、静置,再用分液漏斗分离得到溴的四氯化碳溶液
B.用100mL容量瓶配制50mL0.1mol/LNaOH溶液
C.用托盘天平称取25.30gNaCl
D.用50mL量筒量取4.8mL硫酸
参考答案:A、CCl4与溴水混合后,四氯化碳和水互不相溶,所以溶液分层,,可以采用分液的方法来分离,故A正确;
B、容量瓶的使用规则:配制多大体积的溶液使用多大体积的容量瓶,应该用50mL容量瓶配制50mL0.1mol/LNaOH溶液,故B错误;
C、只能用托盘天平称取25.3g的NaCl,数据精确到小数点后一位,故C错误;
D、用量筒量取和量筒的规格相近体积的溶液,否则误差会很大,故D错误.
故选A.
本题解析:
本题难度:一般
4、填空题 利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程如下:

已知:Zn及其化合物的性质与Al及其化合物的性质相似。请回答下列问题:
(1)用NaOH溶液处理废旧镀锌铁皮可以去除油污,还可以____________________。
(2)调节溶液A的pH可产生Zn(OH)2沉淀,为制得ZnO,后续操作步骤是_____→洗涤→_____。
(3)由溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2,其原因是________________。
(4)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。请写出酸性条件下K2Cr2O7与Fe2+反应的离子方程式?(K2Cr2O7被还原为Cr3+)。
(5)若需配制浓度为0.01000 mol・L-1的K2Cr2O7标准溶液250mL,应准确称取K2Cr2O7?g(保留四位有效数字,已知M(K2Cr2O7)="294.0" g・mol-1)。配制该标准溶液时,下列仪器一定不要用到的有?(用编号表示)。
①电子天平?②烧杯?③量筒 ④玻璃棒 ⑤250 mL容量瓶 ⑥胶头滴管 ⑦托盘天平
(6)若配制K2Cr2O7标准溶液时,俯视刻度线,则测定结果_______(填“偏大”、“偏小”或“不变”,下同);滴定操作中,若滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则滴定结果将________。
参考答案:(1)溶解镀锌层 (2)过滤、灼烧?(3)N2气氛下,防止Fe2+被氧化
(4)6Fe2+ + Cr2O72- + 14H+ =?6Fe3+ + 2Cr3+ + 7H2O?(5)0.7350?③⑦?(6)偏小 ?偏大
本题解析:(1)NaOH溶液能与锌发生反应,所以用NaOH溶液处理废旧镀锌铁皮可以去除油污,还可以溶解镀锌层。(2)反应产生Zn(OH)2沉淀,加热分解产生氧化锌和水。所以为制得ZnO,后续操作步骤是过滤→洗涤→灼烧。(3)氮气化学性质不活泼,在这种惰性环境中可防止Fe2+被氧化。(4)反应的两种方程式是:6Fe2+ + Cr2O72- + 14H+ =?6Fe3+ + 2Cr3+ + 7H2O?(5)m=n・M="0.01mol/L×0.25L×294.0" g/mol=0.7350g.配制物质的量浓度的溶液用到的仪器有①电子天平?②烧杯?③量筒 ④玻璃棒 ⑤250 mL容量瓶 ⑥胶头滴管。(6)若配制K2Cr2O7标准溶液时,俯视刻度线,由于溶液的体积偏小所以K2Cr2O7标准溶液浓度偏大,用这种标准溶液测定,消耗的标准溶液就偏小结果偏小;滴定操作中,若滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,消耗的标准溶液的体积读数偏大则滴定结果将偏大。
本题难度:困难
5、选择题 下列有关实验操作的叙述正确的是 (? )
A.实验室常用图所示的装置制取少量的乙酸乙酯
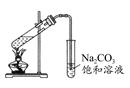
B.用50 mL酸式滴定管可准确量取25.00 mL KMnO4溶液
C.用量筒量取5.00 mL 1.00 mol・L-1盐酸于50 mL容量瓶中,加水稀释至刻度,可配制0.100 mol・L-1盐酸
D.用苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出
参考答案:B
本题解析:A项,图中导管不能插入饱和Na2CO3溶液中;C项,量筒读数只能读到小数点后一位;D项,苯的密度小于水,有机层应在上层。
本题难度:一般