1������� ʵ����Ҫ����1mol/L��ϡ����250mL���ش��������⣺
��1����Ҫ98%�ܶ�Ϊ1.84g/cm3��Ũ���� mL
��2������ʱ������ʹ�õ������� ���������� (�����) ��ȱ�ٵ������� ������ ��
���ձ�����100 mL��Ͳ������20 mL��Ͳ ��1000 mL����ƿ ��250 mL����ƿ����������ƽ(������) �߲�����
��3������ʱ����ʵ�������õ��������������÷ֱ��� �� ��
��4�����ƹ����г��������������������ҺŨ���к�Ӱ�죨�ƫ�ߡ���ƫ�͡�����Ӱ�족��
��û��ϴ���ձ��Ͳ���������������������������
�������ˮ�����˿̶��ߣ�ȡ��ˮʹҺ��ǡ�õ��̶��ߡ�����������������
������ƿû�и������������������
�ο��𰸣���1��13.6��2�֣�����2���٢ۢݢߣ�2�֣�����ͷ�ιܣ�1�֣���
��3�����衢������ÿ��1�֣���
��4��ƫ�͡�ƫ�͡���Ӱ�죨ÿ��2�֣�
�����������1������ϡ��ǰ������������ȿɵã���?V?��=C?V?M��V=13.6mL����2������ʱ������Ͳ��ȡŨ�������ձ���ϡ�ͣ��ò������Ͻ��裬����ȴ��ת�Ƶ�250 mL����ƿ�У���ˮ���������1��2����ʱ���ý�ͷ�ιܶ��ݣ���3������ʱ����ʵ�������õ��������������÷ֱ��ǽ������������4����û��ϴ���ձ��Ͳ�������������ʧ��Ũ��ƫ�ͣ��������ˮ�����˿̶��ߣ�ȡ����ˮ�к������ʣ�Ũ��ƫ�ͣ���ת����Һ֮�����ˮ�����ߣ�ԭ����ˮ��Ӱ�졣
���㣺������Һ�����ƺ���������
�����Ѷȣ�һ��
2�������� ����16.8gNaHCO3��û������ų�ʱ��ʣ���������ʲô������ʣ�����ʵ����������ʵ�����
��1������NaHCO3ʱ�����Ļ�ѧ��Ӧ:___________________________
��2��ʣ���������?������Ϊ?�����ʵ���Ϊ?����д��������̣�
�ο��𰸣���1������NaHCO3ʱ�����Ļ�ѧ��ӦΪ��2NaHCO3 Na2CO3��H2O��CO2����2�֣�?
Na2CO3��H2O��CO2����2�֣�?
��2��ʣ��������Na2CO3��10.6g��0.1mol��4�֣�
���������̼�����Ƽ��ȷֽ��̼���ơ�ˮ�Ͷ�����̼��
2NaHCO3 Na2CO3��H2O��CO2��
Na2CO3��H2O��CO2��
168? 106
16.8g? m(Na2CO3)
106m(Na2CO3)= 16.8g*106
��ã�m(Na2CO3)=10.6g
N(Na2CO3)=10.6g/106(g/mol)=0.1mol
���������⿼����̼�����Ƶ����ʣ���Ŀ���ѽ�𣬿�������Դ���ڽ̲ģ���������ѧ���ļ���������
�����Ѷȣ�һ��
3������� ��3�֣�ͬ��ͬѹ�£�ijƿ��������ʱ����Ϊ116g������������̼ʱ������Ϊ122g����������Aʱ����Ϊ114g��A��Ħ������Ϊ________��
�ο��𰸣�28g/mo
������������ݰ����ӵ����ɿ�֪�����ǵ���������ʵ�������ͬ�ġ������ƿ��������x����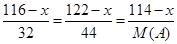 ,���M(A)��28g/mol��
,���M(A)��28g/mol��
�����Ѷȣ�һ��
4��ѡ���� ��Al2��SO4��3��MgSO4��K2SO4�Ļ����Һ�У����е�Al3+��Mg2+��SO42-�ĸ�������2��3��8������Һ��Al2��SO4��3��MgSO4��K2SO4�����ʵ���֮���ǣ�������
A��1��2��4
B��2��3��2
C��1��2��3
D��1��3��2
�ο��𰸣���Һ�ʵ����ԣ��������������������ȣ���K+�ĸ�����Al3+��Mg2+��SO42-�ĸ�������x��2��3��8����x+2��3+3��2=2��8������x=4��ͬһ��Һ�����ӵĸ���֮�ȵ�����Ũ��֮�ȣ��ٸ����仯ѧʽ֪Al2��SO4��3��MgSO4��K2SO4�����ʵ���Ũ��֮��Ϊ22��3��42=1��3��2��ͬһ��Һ�и����ʵ����ʵ���֮�ȵ��������ʵ���Ũ��֮�ȣ�
��ѡD��
���������
�����Ѷȣ���
5��ѡ���� ���ڰ���٤������NA������˵����ȷ���ǣ�?��
A�����³�ѹ�£�1mol�����к��й��ۼ�Ϊ4NA
B����״���£�22.4L�״���ȫȼ�ղ���NA��CO2����
C�����³�ѹ�£�46g NO2��N2O4������У�������ΪNA
D��1L1mol/L Na2CO3��Һ�У������Ӹ�������NA
�ο��𰸣�D
���������
��ȷ�𰸣�D
A������ȷ�����³�ѹ�£�P4��������6�����ۼ���1mol�����к��й��ۼ�Ϊ6NA
B������ȷ����״���£��״�ΪҺ�壻
C������ȷ�����³�ѹ�£�46g NO2��N2O4������У�����������NA
D����ȷ��1L1mol/L Na2CO3��Һ�У�CO32�DҪˮ�⣬�����Ӹ�������NA
�����Ѷȣ�һ��