1、选择题 下列叙述中,正确的是(?)
A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同
B.原子最外层电子数为2的元素一定处于周期表IIA族
C.离子化合物中可能含有共价键,但共价化合物中一定不含离子键
D.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
参考答案:C
本题解析:两种微粒,若核外电子排布完全相同,则其化学性质不一定相同,例如Na+和F-;原子最外层电子数为2的元素可以是He或者是副族、第Ⅷ族元素;离子化合物中可能含有共价键,例如NaOH,但共价化合物中一定不含离子键;单原子形成的离子,一定具有稀有气体元素原子的核外电子排布,例如Fe2+、H+等。所以正确的答案是C。
本题难度:简单
2、选择题 Q、W、X、Y、Z都是短周期元素。X、Y、Q在周期表中的位置关系如图。W、Z的最外层电子数相同,Z的核电荷数是W的2倍。则下列说法不正确的是? ( )。
?
A.非金属性:W>Z
B.原子半径:X>Y>Z
C.最高价氧化物对应水化物的碱性:X>Y
D.氢化物稳定性:Q>W
参考答案:D
本题解析:由于X、Y、Q是短周期元素,由X、Y、Q在周期表中的相对位置可知Q为C、X为Na、Y为Al;W、Z的最外层电子数相同,Z的核电荷数是W的2倍,则W是O、Z是S,故D不正确。
本题难度:一般
3、填空题 如图为四、五、六、七主族元素简单氢化物沸点随周期变化图像,(代表氢化A、B、C、D物中另外一种元素)分析图像并回答
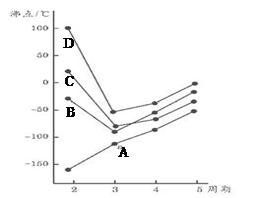
(1)写出B3-的空间构型?
(2)B元素另外一种氢化物可做火箭的燃料,其电子式为:__________________,中心原子杂化方式为_______________
(3)A元素氧化物晶体类型为____________________,研究发现其氧化物晶胞中,A的位置与金刚石晶胞中碳原子位置相似,试分析晶胞中占有氧原子个数应为___________个。
(4)A、B、C、D第一电离能由小到大的顺序是____________________(用元素符号表示)
参考答案:(1)直线形?
(2) ? sp3杂化?
? sp3杂化?
(3)原子晶体? 16?
(4)Si<O<N<F
本题解析:由图像和题意可知A、B、C、D分别为:SiH4、NH3、HF、H2O
(1)B3-为N3-故空间构型为直线形?
(2)B元素另外一种氢化物可做火箭的燃料故为N2H4,电子式略、? sp3杂化?
(3)A元素氧化物为SiO2故晶体类型为原子晶体; 其氧化物晶胞中,A的位置与金刚石晶胞中碳原子位置相似,故每个晶胞中占有的Si原子数为8,根据SiO2可知O原子数为16。?
(4)根据第一电离能规律由小到大的顺序为Si<O<N<F
本题难度:一般
4、选择题 X元素的简单阳离子和Y元素的简单阴离子具有与氩原子相同的电子层结构。下列叙述正确的是(? )
A.X的原子序数比Y的小
B.X原子的电子层数比Y的少
C.X的原子半径比Y的小
D.X元素的最高正价比Y的小
参考答案:D
本题解析:X元素的简单阳离子和Y元素的简单阴离子具有与氩原子相同的电子层结构,说明Y元素在X元素的上一周期,X的原子序数比Y的大。
本题难度:简单
5、选择题 月球的土壤中含有较丰富的质量数为3的氦,它可以作为未来核聚变的重要原料之一。氦的该种核素为
A.1 1He
B.3 2He
C.5 2He
D.1 2He
参考答案:B
本题解析:考查原子的组成及表示方法。在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数。氦的质子数是2,所以选项B正确,答案选B。
本题难度:简单