1、选择题 欲配制100 mL 1.0 mol/L Na2SO4溶液,正确的方法是
①将14.2 g Na2SO4溶于100 mL水中
②将32.2 g Na2SO4・10H2O溶于少量水中,再用水稀释至100 mL
③将20 mL5.0 mol/L Na2SO4溶液用水稀释至100 mL
A.①②
B.②③
C.①③
D.①②③
参考答案:B
本题解析:①错,因不知道溶液的体积,无法计算;②正确,100 mL 1.0 mol/L Na2SO4溶液的物质的量为0.1 mol,而32.2 g Na2SO4・10H2O的物质的量也为0.1mol,溶液体积为0.1L;③正确;20 mL5.0 mol/L Na2SO4溶液的物质的量为0.1 mol;
本题难度:简单
2、选择题 在中学化学实验中,对某些化学试剂进行循环再用,可以节省资源、减少污染、降低实验成本,下列做法合理的是
编号
| 实验名称
| 回收试剂
| 回收方法
| 回收后用途
|
①
| 氧气制法
| 二氧化锰
| 溶解、过滤、洗涤、干燥
| 重复使用
|
②
| 铁和硫反应
| 硫化亚铁
| 直接密封保存
| 制硫化氢
|
③
| 萃取
| 四氯化碳
| 碱液洗涤、分液
| 重复使用
|
④
| 氨的喷泉实验
| 稀氨水
| 直接密封保存
| 氨水的性质实验
|
⑤
| 浓硫酸的稀释
| 稀硫酸
| 直接密封保存
| 制氢气、硫酸根检验等
|
A.①③④⑤
B.①②③④⑤
C.①③⑤
D.①②④⑤
参考答案:A
本题解析:铁与硫反应虽生成硫化亚铁,但同时混有铁或硫,铁与酸反应生成H2,使制得的硫化氢不纯。
本题难度:简单
3、实验题 对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺磺化得到。
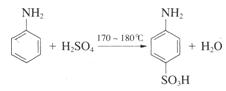
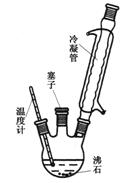
实验室可利用下图实验装置合成对氨基苯磺酸。实验步骤如下:
①?在一个250 mL三颈烧瓶中加入10 mL苯 胺及几粒沸石,
胺及几粒沸石,
将三颈烧瓶放入冷水中冷却,小心地加入18 mL浓硫酸 。
②?将三颈烧瓶置于油浴中缓慢加热至170~180℃,维持此温度2~2.5 h。
③ 将反应液冷却至约50℃后,倒入盛有100 mL冷水的烧杯中,用玻璃棒不断搅拌,促使晶体析出,抽滤,用少量冷水洗涤,得到的晶体是对氨基苯磺酸粗产品。
④ 将粗产品用沸水溶解,冷却结晶(若溶液颜色过深,可用活性炭脱色),抽滤,收集产品,晾干。(说明:100 mL水在20℃时可溶解对氨基苯磺酸1.08 g,在100℃时可溶解6.67 g。)
试回答填空。
(1)装置中冷凝管的作用是?▲?。
(2)步骤②中采用油浴加热,下列说法正确的是?▲?(填序号)。
A.用油浴加热的好处是反应物受热均匀,便于控制温度
B.此处也可以改用水浴加热
C.实验装置中的温度计可以改变位置,也可使其水银球浸入在油中
(3)步骤③用少量冷水洗涤晶体的好处是?▲?。
(4)步骤③和④均进行抽滤操作,在抽滤完毕停止抽滤时,应注意先?▲?,
然后?▲?,以防倒吸。
(5)步骤④中有时需要将“粗产品用沸水溶解,冷却结晶,抽滤”的操作进行多次,其目的是?。每次抽滤后均应将母液收集起来,进行适当处理,其目的是?▲?。
参考答案:(共12分)(1)冷凝回流(1分)?
(2)AC(2分,有错得0分,漏选给1分)
(3)减少氨基苯磺酸的损失(1分)
(4)拆下连接泵和吸滤瓶的橡皮管(2分)关闭水龙头(2分)
(5)提高对氨基苯磺酸的纯度(2分)?提高氨基苯磺酸的产率(2分)
本题解析:略
本题难度:一般
4、选择题  在测定硫酸铜晶体结晶水含量的实验中,下列操作会引起测量结果偏小的是(? )
在测定硫酸铜晶体结晶水含量的实验中,下列操作会引起测量结果偏小的是(? )
A.加热前称量时坩埚未完全干燥
B.加热时间过长,晶体部分变黑
C.加热过程中有少量晶体溅出
D.粉末未完全变白就停止加热
参考答案:D
本题解析:略
本题难度:简单
5、选择题 下列有关叙述中正确的是
A.滴定管下端连有橡皮管的为酸式滴定管
B.用已知物质的量浓度的盐酸滴定未知物质的量浓度的碱溶液(甲基橙作指示剂),记录标准液起始体积时,仰视读数,终点时俯视读数,导致误差偏高。
C.滴定前应首先排除尖嘴部分的气泡。
D.滴定过程中两眼应注视滴定管内液面的变化。
参考答案:C
本题解析:略
本题难度:一般