1、选择题 下列有关比较中,大小顺序排列错误的是
[? ]
A.热稳定性:HF>H2O>H2S
B.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
C.酸性:H4SiO4<H3PO4<H2SO4<HClO4
D.沸点:SiC>NaCl>Si>I2
参考答案:D
本题解析:
本题难度:一般
2、填空题 请回答下列问题:
(1)已知石墨晶体是平面六边形层状结构,其最小碳环是_______元环,一个碳原子被______个最小环共用,该晶体中,碳原子数与C-C键的数目之比为____________;层与层之间的作用属于____________。
(2)水分子内的O-H键(代码是a)、分子间的范德华力(代码是b)、分子间氢键(代码是c)由强到弱的顺序为_______________。(用代码填充)
(3)对羟基苯甲醛的沸点高于邻羟基苯甲醛的原因是_____________________。
(4)某晶体仅有一种元素组成,其密度为5g/cm3,用X射线研究该晶体的结果表明,在边长为1×10-7cm的立方体中仅有20个原子,则此元素的相对原子质量约为____________。
参考答案:
(1)六;3;2:3;范德华力
(2)a>c>b?
(3)前者存在分子间氢键,后者存在分子内氢键?
(4)150.5
本题解析:
本题难度:一般
3、填空题 键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。参考以下表格的键能数据,回答下列问题

(1)比较下列两组物质的熔点高低(填“>”或“<”) SiC__________Si; SiCl4___________SiO2
(2)如图立方体中心的“ ”表示金刚石晶体中的一个原子,请在立方体的顶点用“
”表示金刚石晶体中的一个原子,请在立方体的顶点用“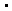 ”表示出与之紧邻的碳原子
”表示出与之紧邻的碳原子
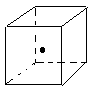
(3)工业上高纯硅可通过下列反应制取:SiCl4(g) + 2H2(g) Si(s)+4HCl(g) 计算该反应的反应热△H为______ kJ/mol。
Si(s)+4HCl(g) 计算该反应的反应热△H为______ kJ/mol。
参考答案:(1)>;<
(2)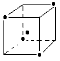 或
或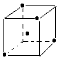
(3)+236
本题解析:
本题难度:一般
4、选择题 科学家在高压下成功地将CO2转化为具有类似SiO2结构的晶体,下列关于CO2的原子晶体的说法正确的是
[? ]
A.CO2的分子晶体转化为原子晶体是化学变化
B.CO2的原子晶体和分子晶体实际上是同种物质
C.CO2的原子晶体和分子晶体具有相同的物理性质
D.在CO2的原子晶体中,每一个C原子周围结合4个O原子
参考答案:AD
本题解析:
本题难度:简单
5、选择题 美国Lawtcce?Lirermre国家实验室的V?Lota?C?S?Yoo和H?Cynn成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2原子晶体的说法正确是( )
A.CO2的原子晶体和分子晶体互为同素异形体
B.在一定条件下,CO2原子晶体转化为分子晶体是化学变化
C.CO2的原子晶体和CO2分子晶体具有相同的物理性质
D.CO2的原子晶体中,每个碳周围结合4个氧原子,每一个氧原子跟两个碳原子相结合
参考答案:A、同素异形体的研究对象是单质.CO2是化合物,不是单质,故二者不互为同素异形体,故A错误;
B、CO2原子晶体转化为CO2分子晶体,结构已发生改变,且二者的性质也有较大差异,故二者是不同的物质,二者的转变是化学变化,故B正确;
C、CO2原子晶体与CO2分子晶体,结构不同,二者是不同的物质,物理性质不同,如CO2原子晶体硬度很大,CO2分子晶体硬度不大,故C错误;
D、CO2原子晶体与SiO2结构类似,每个碳原子与4个氧原子通过1对共用电子对连接,每个氧原子与2个碳原子通过1对共用电子对连接,故D正确.
故选BD.
本题解析:
本题难度:一般