1��ѡ���� ���������ܰ����������ǿ����ʡ�������ʡ��ǵ���ʵ������ȷ���ǣ�������
| ? | ������ | ����� | ǿ����� | ������� | �ǵ����
A
����
ˮú��
����
����
H2
B
����
ʯ��ˮ
���ᱵ
HNO2
NH3
C
���
������Һ
�Ȼ���
��ˮ
��������
D
������
Ư��
���Լ�
�Ȼ���
�Ҵ�
|
A��A
B��B
C��C
D��D
�ο��𰸣�A�����ᡢˮú�������ᡢ���ᡢ��ˮ��H2�ֱ����ڻ�������ǿ����ʡ�������ʣ����ʣ���A����
B��������ʯ��ˮ�����ᱵ��HNO2��NH3�ֱ����ڻ��������ǿ����ʡ�������ʣ��ǵ���ʣ���B��ȷ��
C����������Һ���Ȼ��ơ���ˮ����������ֱ����ڻ��������ǿ����ʡ������ǵ���ʣ���C����
D�������ᡢƯ�ۡ����Լء��Ȼ��⡢�Ҵ��ֱ����ڻ��������ǿ����ʡ�ǿ����ʣ��ǵ���ʣ���D����
��ѡ��B��
���������
�����Ѷȣ�һ��
2��ѡ���� ��ͼ��ʾ�������ʻ�����Ĵ�����ϵ���±��еĴ�����ϵ����ȷ����

?
| ? Z
| ? Y
| ? X
|
��
| ������
| ������
| ������
|
A
| ������ԭ��Ӧ
| �û���Ӧ
| ��ѧ��Ӧ
|
B
| ����
| ��ɢϵ
| �����
|
C
| ���ӻ�����
| �����
| ������
|
D
| ���Թ��ۼ�
| ���ۼ�
| ��ѧ��
�ο��𰸣�A
���������������ԭ��Ӧ��һ�������û���Ӧ��A����ȷ���������ȷ�ģ���ѡA��
�����Ѷȣ���
3��ѡ���� ������ڻ�ѧѧ�Ƶķ�չ�����˷dz���Ҫ�����á����з������������
��?������������Ԫ�����࣬�����ʷ�Ϊ���ʡ��������
��?���ݷ�Ӧ���Ƿ��е��ӵ�ʧ������ѧ��Ӧ��Ϊ������ԭ��Ӧ�ͷ�������ԭ��Ӧ
��?���ݷ�ɢϵ�Ƿ���ж����������ɢϵ��Ϊ��Һ���������Һ
��?���������ڷ�Ӧ�еõ������Ķ��٣�����������Ϊǿ����������ǿ������
A����
B���٢�
C���٢ڢ�
D���ڢۢ�
�ο��𰸣�A
������������ݷ�Ӧ���Ƿ��е���ת�ƣ�����ѧ��Ӧ��Ϊ������ԭ��Ӧ�ͷ�������ԭ��Ӧ���ڲ���ȷ�����ݷ�ɢϵ�з�ɢ����ֱ����С�IJ�ͬ������ɢϵ��Ϊ��Һ���������Һ���۲���ȷ�������Ե�ǿ����õ����ӵ����׳̶��й�ϵ��������ӵĶ�����ϵ���ܲ���ȷ����ѡA��
�����������Ǹ߿��еij������ͣ����ڻ���������Ŀ��顣���������ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ�����ѶȲ�����Ĺؼ�����ȷ���ʵķ������Ȼ��������ü��ɡ�
�����Ѷȣ�һ��
4��ѡ���� ���и����е�������������ʱ����Ӧ�����ı��Ӧ�������ı䣬���������������仯���ǣ�������
A��Na��O2
B��Fe��Cl2
C��Na2O2��CO2
D��C��O2
�ο��𰸣�A��Na��O2��Ӧ���¶Ȳ�ͬ�����ﲻͬ�����������������ƣ���ȼ���ɹ������ƣ���A����
B��Fe��Cl2�ķ�Ӧ�¶Ȳ�ͬ������ͬ�����������ĸı䣬��B��ȷ��
C��Na2O2��CO2�ķ�Ӧ���¶Ȳ�ͬ������ͬ�����������ĸı䣬��C��ȷ��
D��ľ̿��������Ӧ����������ʱ���ɶ�����̼����������ʱ����һ����̼����Ӧ�������ȸı䣬��������������ı䣬��D����
��ѡ��BC��
���������
�����Ѷȣ�һ��
5������� ���ʵķ�����У�������෨����״���෨�ȶ��ַ��������ж��������������ͼ��
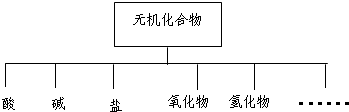
��1����ͼ��ʾ�����ʷ����������______��
��2����K��Na��H��O��S��N�������ֻ�����Ԫ����ɺ��ʵ����ʣ��ֱ������±��Тڡ��ܡ����森
| ������� | �� | �� | �� | ������ | �⻯��
��ѧʽ
��HNO3
��______
��NaOH
��______
��Na2SO4
��______
��SO2
��SO3
��NH3
|
��3��д����������Ģ���Һ��Ӧ�����ӷ���ʽ______��
��4��3Cu+8HNO3��ϡ���T3Cu��NO3��2+2NO��+4H2O��Ӧ�У���������______������������______������3molCu��ȫ��Ӧ��ת�Ƶ�����Ϊ______mol��
��5��ʵ�����Ʊ���Ļ�ѧ����ʽΪ______��
�ο��𰸣���1����״���෨��һ�ֺ�����ķ��෨�����ղ�Σ�һ��һ�����֣�����һ�ô�������Ҷ��֦���ˡ�����ͼʾ����������״ͼ���ʴ�Ϊ����״���෨��
��2����������������ȫ���������ӵĻ������H2SO4����������������ȫ��Ϊ���������ӣ���NaOH���ε������������Ϊ�������ӣ�������Ϊ������ӣ���KNO3��
�ʴ�Ϊ����H2SO4����NaOH����KNO3��
��3������������������Ʒ�Ӧ����ˮ���������ƣ��䷴Ӧ�����ӷ���ʽΪ��SO2+2OH-�TSO32-+H2O���ʴ�Ϊ��SO2+2OH-�TSO32-+H2O��
��4��3Cu+8HNO3��ϡ���T3Cu��NO3��2+2NO��+4H2O��Ӧ�У�NԪ�صĻ��ϼ۽��ͣ�������������HNO3��ͭԪ�ػ��ϼ����ߣ��ǻ�ԭ����Ӧ��������������������������� Cu��NO3��2��Cu��0�����ߵ�+2��ʧȥ2�����ӣ���������3mol Cu��ȫ��Ӧ��ת�Ƶ�����Ϊ6mol��
�ʴ�Ϊ��HNO3��Cu��NO3��2�� 6��
��5��ʵ�����ü����������ƺ��Ȼ�粒�������ķ�������ȡ�������䷴Ӧ�Ļ�ѧ����ʽΪ��Ca��OH��2+2NH4Cl��.CaCl2+2H2O+2NH3����
�ʴ�Ϊ��Ca��OH��2+2NH4Cl��.CaCl2+2H2O+2NH3����
���������
�����Ѷȣ���
|