1������� ��֪X��Y��Z��W����Ԫ����Ԫ�����ڱ�������������ͬ�����ڵ�Ԫ�أ���ԭ��������������X��Wͬ���壬Y��ZΪͬ���ڵ�����Ԫ�أ�Wԭ�ӵ�����������Y��Zԭ������������֮�ͣ�Y���⻯���������3�����ۼ���Zԭ�������������Ǵ�����������3�������ƶϣ�
��1��X��Y��Z��W����Ԫ�ص����ƣ�Y______��W______
��2��������Ԫ���е�����Ԫ����ɵ�������ˮ��ˮ��Һ�Լ��ԵĻ�����ĵ���ʽ�ֱ�Ϊ
______��
��3����X��Y��Z���γɵ����ӻ�������W������������ˮ�����Ũ��Һ����ʱ��Ӧ�����ӷ���ʽ��______��
��4����X��Y�γɵĻ�����XY5����______���壬д��XY5��ˮ�ķ�Ӧ����ʽ______��
�ο��𰸣���1��Y���⻯���������3�����ۼ���YӦΪNԪ�أ�Zԭ�������������Ǵ�����������3������ZΪOԪ�أ�Wԭ�ӵ�����������Y��Zԭ������������֮�ͣ���WΪNaԪ�أ�X��Wͬ���壬��ԭ��������С��ΪHԪ�أ��ʴ�Ϊ�������ƣ�
��2��������Ԫ���е�����Ԫ����ɵ�������ˮ��ˮ��Һ�Լ��ԵĻ�����ֱ��ǰ����������Լ��������ƣ������ʽ�ֱ�Ϊ��
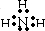
��

��
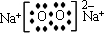
���ʴ�Ϊ��
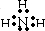
��

��
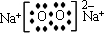
��
��3����X��Y��Z���γɵ����ӻ�����ΪNH4NO3��W������������ˮ����ΪNaOH�������ڼ���������Ӧ���ɰ�����
��Ӧ�����ӷ���ʽΪNH4++OH-?��?.?NH3��+H2O���ʴ�Ϊ��NH4++OH-?��?.?NH3��+H2O��
��4��Y�γɵĻ�����XY5�������Ӿ��壬ΪNH4H������-1�۵�HԪ�أ�����ǿ��ԭ�ԣ���ˮ��Ӧ������������Ӧ�Ļ�ѧ����ʽΪNH4H+H2O�TNH3?H2O+H2����
�ʴ�Ϊ�����ӣ�NH4H+H2O�TNH3?H2O+H2����
���������
�����Ѷȣ�һ��
2������� ��A��B��C��D����Ԫ�أ�AԪ���ǵؿ��к������Ľ���Ԫ�أ�BԪ�ص�ԭ����M���������L����1�����ӣ�CԪ�ص�ԭ�ӵõ�2�����ӣ�DԪ�ص�ԭ��ʧȥ1�����ӣ����õ���������������ԭ����ͬ�ĵ��Ӳ�ṹ���ش��������⣺
��1����������Ԫ�ص����Ʒֱ���A______B______C______D______��
��2������A���ӡ�Cԭ�ӵĽṹʾ��ͼ______��______��
�ο��𰸣�A��B��C��D����Ԫ�أ�AԪ���ǵؿ��к������Ľ���Ԫ�أ���AΪAlԪ�أ�BԪ�ص�ԭ����M���������L����1�����ӣ���M�������Ϊ8-1=7����BΪClԪ�أ�CԪ�ص�ԭ�ӵõ�2�����ӣ�DԪ�ص�ԭ��ʧȥ1�����ӣ����õ���������������ԭ����ͬ�ĵ��Ӳ�ṹ����Cԭ�Ӻ��������Ϊ10-2=8��ΪOԪ�أ�DԪ��ԭ�Ӻ��������Ϊ10+1=11����DΪNaԪ�أ�
��1��������������֪��AΪ����BΪ�ȣ�CΪ����DΪ�ƣ��ʴ�Ϊ�������ȣ������ƣ�
��2��A����ΪAl3+�����������Ϊ10����2�����Ӳ㣬����������Ϊ8�����ӽṹʾ��ͼΪ
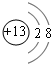
��
CΪ��Ԫ�أ�ԭ�Ӻ��������Ϊ8��ԭ�ӽṹʾ��ͼΪ
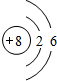
��
�ʴ�Ϊ��

��
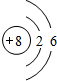
��
���������
�����Ѷȣ���
3������� ��A��B��C��D��E��������Ԫ�أ���ԭ�ӵ���������������Ϊ1��3��7��6��4��ԭ?����?����E��B��D��C��A��˳����������D��������������Է�����������̬�⻯�����Է�������֮��Ϊ2.35��1���Ҹ�ԭ�Ӻ������Ӻ�������ȣ�A��B��Cԭ�ӵĴ���㶼��8�����ӣ�Eԭ�ӵĴ������2?�����ӣ�
��1������D��Ħ������______��д��D��ԭ�ӷ���______
��2��д��A�ĵ�����CuSO4��Һ��Ӧ�������ӷ���ʽ______��
E�ĵ�����D������������Ӧˮ���ﷴӦ�Ļ�ѧ����ʽΪ______��
��3��C��D��E��Ԫ������������Ӧˮ�����������ǿ������˳��Ϊ______��
��4��B������������Ӧˮ�����A��C��Ԫ�ص�����������Ӧˮ����ֱ�Ӧ�����ӷ���ʽΪ��B��A______��
B��C______��
�ο��𰸣��ȸ�����Ϣ�ƶ�Ԫ�أ�D���������6�����ӣ��������������ɱ�ʾΪDO3���⻯��ɱ�ʾΪH2D����D�����
ԭ������Ϊx������D��������������Է�����������̬�⻯�����Է�������֮��Ϊ2.35��1����ʽ��x+482+x=2.35��1��
��ã�x=32����Dԭ�Ӻ�������������������ȣ�����D��������Ϊ16��ΪSԪ�أ�Eԭ�ӵĴ������2?��������
�������4�����ӣ�����EΪCԪ�أ�B�������3�����ӣ�ԭ����������E��D֮�䣬����BΪAlԪ�أ�A��B��Cԭ��
�Ĵ���㶼��8�������������ֱ���1��7�����ӣ�����AΪKԪ�أ�CΪClԪ�أ�
��1����Ħ��������g/molΪ��λʱ��ֵ�������ԭ��������ȣ��ʴ�Ϊ��32g/mol��?3216S��
��2��������ˮ�����û���Ӧ��2K+2H2O=2K++2OH-+H2����KOH��������ͭ�������ֽⷴӦ��2OH-+Cu2+=Cu��OH��2����
��ʽ��ӵ��ܷ�Ӧʱ��2K+2H2O+Cu2+=2K++Cu��OH��2+H2����Ũ�������ǿ�����ԣ����C����Ϊ������̼����������ԭΪ��������ӦΪC+2H2SO4��Ũ��?��?.?CO2��+2SO2��+2H2O��
�ʴ�Ϊ��2K+2H2O+Cu2+=2K++Cu��OH��2+H2����C+2H2SO4��Ũ��?��?.?CO2��+2SO2��+2H2O��?
��3����ǽ�����Cl��S��C���������Դ�С˳��Ϊ��HClO4��H2SO4��H2CO3���ʴ�Ϊ��HClO4��H2SO4��H2CO3��?
��4����������Ϊ�����������������ǿ�ᷴӦ������ǿ�Ӧ��B��A��Ӧ��ѧ����ʽΪ��Al��OH��3+KOH�TKAlO2+2H2O��
B��C��Ӧ����ʽΪ��Al��OH��3+3HClO4�TAl��ClO4��3+3H2O�������ӷ���ʽΪAl��OH��3+OH-�TAlO2-+2H2O��Al��OH��3+3H+�TAl3++3H2O��
�ʴ�Ϊ��Al��OH��3+OH-�TAlO2-+2H2O��Al��OH��3+3H+�TAl3++3H2O��
���������
�����Ѷȣ�һ��
4��ѡ���� X��Y��ΪԪ�����ڱ���ǰ20��Ԫ�أ�������ӵĵ��Ӳ�ṹ��ͬ������˵����ȷ���ǣ�������
A����mXa+��nYb-����m+a=n-b
B��X2-�Ļ�ԭ��һ������Y-
C��X��Yһ������ͬ����Ԫ��
D����X��ԭ�Ӱ뾶����Y������̬�⻯����ȶ���HmXһ������HnY
�ο��𰸣�A����mXa+��nYb-�����ӵĵ��Ӳ�ṹ��ͬ��������������ͬ������m-a=n+b����A����
B�������ӵĵ��Ӳ�ṹ��ͬ��X��Yλ��ͬ���ڣ�Ϊ�ǽ���Ԫ�أ�Y��ԭ����������X2-�Ļ�ԭ��һ������Y-����B��ȷ��
C�������ӵĵ��Ӳ�ṹ��ͬ��X��Y��Ϊ�����ӡ����Ϊ��������ͬһ���ڣ���һ��Ϊ������һ��Ϊ�����ӣ���һ������ͬһ���ڣ���C����
D�������ӵĵ��Ӳ�ṹ��ͬ��X��ԭ�Ӱ뾶����Y��X����Ϊ������������̬�⻯���D����
��ѡB��
���������
�����Ѷȣ�һ��
5��ѡ���� ��ͨ�����бز����ٵIJ����ǻ�����뵼�塣������Ϊ�ռ��Ļ�����뵼�������֣�һ��������뵼 �壬��������Я�绰�����ߵ�ͨ�ŷ��������������һ�ֻ�����뵼���ɱ���(Ga)��18�����ӵ�Ԫ��A������(As)ͬ���ҵ��Ӳ������һ���Ԫ��B��ɣ�������Ϊͨ�ŵ����й��ź�ת��Ϊ���źŵ��м���������˻�����Ļ�ѧʽΪ
[? ]
A.GaP
B.AlP
C.GaAs
D.InP
�ο��𰸣�D
���������
�����Ѷȣ���