1、填空题 下图为细菌冶铜和火法冶铜的主要流程。
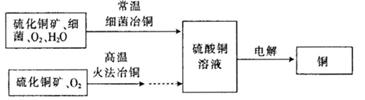
(1) 硫酸铜溶液一般呈________(填“酸”、“碱”或“中”)性,原因是________ (用离子方程式表示)。写出电解硫酸铜溶液的化学方程式:______________(电解过程中,始终无氢气产生)。
(2)细菌冶金又称微生物浸矿,是近代湿法冶金工业上的一种新工艺。细菌冶铜与火法冶铜相比,优点为________________(写出一点即可)。
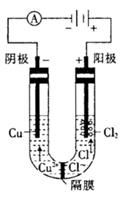
(3) 用惰性电极分别电解浓的氯化铜溶液和硫酸铜溶液。电解浓的氯化铜溶液时发现阴极有金属铜生成,同时阴极附近会出现棕褐色溶液。而电解硫酸铜溶液时,没有棕褐色溶液生成。下面是关于棕褐色溶液成分的探究:
①有同学认为,阴极附近出现的棕褐色溶液是氯气反应的结果,你认为他的猜测是否正确?________(填“正确”或“不正确"),原因是__________
资料1:
一般具有混合价态(指化合物中同一元素存在两种不同的化合价,如Fe3O4中的 Fe元索)的物质的颜色比单一价态的物质的颜色要深。
资料2:
CuCl微溶于水,能溶于浓盐酸。
②猜想:棕褐色溶液中可能含有的离子是________(填3种主要离子符号)。
③验证猜想:完成实验方案(配制棕褐色溶液)。
取少量________固体于试管中,加入________使其溶解,再加入________溶液,观察现象。
④已知电解前,U形管中加入了________100mL0.5 mol . L-1 CuCl2溶液,电解结
参考答案:
本题解析:
本题难度:困难
2、选择题 下列有关电解池说法不正确的是( )
A.电解池是将电能转化为化学能的装置
B.与电源正极相连的是电解池的阴极
C.与电源负极相连的是电解池的阴极
D.在电解池中阳极发生氧化反应
参考答案:B
本题解析:依据电解的原理及电解池的有关知识很易得出答案。
本题难度:简单
3、选择题 用铂作电极电解下列溶液,当消耗相同电量时,在阴极上有金属析出且溶液的pH下降的是
A.KCl
B.CuCl2
C.CuSO4
D.HCl
参考答案:C
本题解析:在阴极上有金属析出,则溶液中须有不活泼金属阳离子,排除AD选项。电解CuCl2生成铜和氯气,放电完毕体系中只剩下水,显中性,故电解过程pH增大,B错。电解CuSO4会生成硫酸,溶液的pH下降,故选C
本题难度:一般
4、选择题 用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是(?)
A.NaCl溶液
B.HCl溶液
C.稀NaOH溶液
D.酸性AgNO3溶液
参考答案:C
本题解析:用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2,这说明电解的实质是电解水,则选项C正确。A中电解产物是氯气、氢气和氢氧化钠,B中电解产物是氯气和氢气。D中电解产物是银、氧气和硝酸,答案选C。
点评:该题是高考中的常见考点和题型,属于中等难度的试题。试题综合性强,在注重对教材基础知识巩固和训练的同时,侧重对学生能力的培养和解题方法的指导和训练。该题的关键是明确电解的工作原理以及离子的放电顺序,然后灵活运用即可。
本题难度:简单
5、简答题 如图为电解装置,X、Y为电极材料,a为电解质溶液.
(1)若a为含有酚酞的KCl溶液,X为Fe,Y为石墨,电解一段时间后:X电极附近可观察到的实验现象是______,写出Y电极的电极反应式______
(2)若要实现Cu+H2SO4=CuSO4+H2↑,则Y电极材料是______,写出X电极的电极反应式______
(3)若要利用该装置在铁制品表面镀上一层银,则a为______,反应前两电极的质量相等,反应后电极质量相差2.16g,则该过程理论上通过电流表的电子数为______.
(4)若X、Y均为惰性电极,a为NaOH溶液,电解一段时间后,溶液的pH______(填“增大”“不变”“减小”),若要使溶液恢复原来的状态,可往溶液中加入______.

参考答案:(1)若a为含有酚酞的KCl溶液,X为Fe,Y为石墨,X电极上氢离子得到电子生成氢气,电极附近溶液中氢氧根离子浓度增大,遇酚酞变红色;Y电极上氯离子失电子生成氯气,电极反应是2Cl--2e-=Cl2↑;
故答案为:电极表面产生气体,附近溶液变红;2Cl--2e-=Cl2↑;
(2)要实现Cu+H2SO4=CuSO4+H2↑,需要利用电解原理,Y电极应是铜做阳极,X电极上是氢离子得到电子生成氢气,阴极电极反应2H++2e-=H2↑;
故答案为:Cu,2H++2e-=H2↑;
(3)利用该装置在铁制品表面镀上一层银,银做阳极Y,铁做阴极X,含银离子的电解质溶液硝酸银溶液进行电解完成,阳极电极反应和电子守恒计算电子转移数,反应前两电极的质量相等,反应后电极质量相差2.16g,依据电子守恒可知,阳极质量减小阴极质量增加的质量相同,阴极析出银的质量=阳极溶解减小的银的质量=1.08g,析出银物质的量=1.08g108g/mol=0.01mol,则该过程理论上通过电流表的电子数为0.01NA或6.02×1021;
故答案为:AgNO3溶液,0.01NA或6.02×1021;
(4)X、Y均为惰性电极,a为NaOH溶液,实质是电解水,溶液浓度增大,溶液PH增大;氢氧根离子在阳极上失电子发生氧化反应,氢离子在阴极得到电子发生还原反应生成氢气,恢复溶液浓度依据出什么,加什么的原则分析,应加入水恢复溶液浓度;
故答案为:增大,H2O;
本题解析:
本题难度:一般