1、选择题 设NA表示阿伏加德罗常数,下列叙述正确的是
[? ]
A.1.7g?OH-?所含电子数为0.9NA?
B.标准状况下,11.2?L?HCl?所含质子数为18NA
C.常温下,11.2?L?Cl2所含原子数为NA?
D.0.5?mol?D2O?中所含质子数为5NA
参考答案:D
本题解析:
本题难度:简单
2、选择题 用NA表示阿伏加德罗常数的值,下列叙述中错误的是( )
A.标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA
B.室温下,21.0g乙烯和丁烯的混合气体含有的碳原子数目为1.5NA
C.等物质的量的甲基(-CH3)与羟基(-OH)所含电子数相等
D.1mol乙烷含有的共价键数目为8NA
参考答案:A、标况下,22.4LCH4的物质的量是1mol,一个甲烷分子中含有10个电子,所以1mol甲烷中含有10NA个电子;18g水的物质的量是1mol,一个水分子中含有10个电子,所以所以1mol水分子中含有10NA个电子,故A正确.
B、乙烯和丁烯的最简式相同,都是CH2,21.0g乙烯和丁烯的混合气体中含有CH2的物质的量是1.5mol,一个CH2中含有1个碳原子,所以21.0g乙烯和丁烯的混合气体含有的碳原子数目为1.5NA,故B正确.
C、一个甲基(-CH3)中含有9个电子,一个羟基(-OH)9个电子,所以等物质的量的甲基(-CH3)与羟基(-OH)所含电子数相等,故C正确.
D、一个乙烷分子是含有7个共价键,1mol乙烷含有的共价键数目是7NA,故D错误.
故选D.
本题解析:
本题难度:一般
3、选择题 设Na表示阿伏加德罗常数,下列叙述正确的是
A.23 gNO2和23 gN2O4所含原子数目均为1.5Na
B.18 gD2O所含电子数目为10Na
C.标准状况下,22.4 LH2O所含分子数目为Na
D.1 L1 mol・L-1的两种强酸溶液中,所含氢离子数目均为Na
参考答案:A
本题解析:B中D2O的摩尔质量为20 g・mol-1,所以它含有的电子的数目为9Na;由于水在标准状况下为液体,所以C选项错误;D中需要考虑酸的元数.
本题难度:简单
4、选择题 设NA表示阿伏加德罗常数的值,下列说法不正确的是
[? ]
A.常温常压下,0.05NA个CO2分子所占的体积是1.12?L
B.氨气的摩尔质量和NA个氨分子的质量在数值上相等
C.2?g重氢气(D2)在标准状况下所含原子个数为2NA
D.常温常压下,32?g氧气与34?g硫化氢分子个数比为1∶1?
参考答案:AC
本题解析:
本题难度:简单
5、选择题 设NA为阿伏伽德罗常数的数值,下列说法正确的是
A.常温下,23gNO2含有NA个氧原子
B.1L0.1mol?L-1的烧碱溶液中含有0.1NA个OH-
C.常温常压下,22.4LCCl4含有个NACCl4分子
D.1molFe与足量的盐酸反应,转移3NA个电子
参考答案:AB
本题解析:分析:A、根据N=nNA= NA结合分子构成计算.
NA结合分子构成计算.
B、根据n=CV结合化学式构成计算.
C、根据气体摩尔体积的使用范围及条件分析.
D、根据铁与转移电子之间的关系式计算.
解答:A、23gNO2含有二氧化氮分子的个数N=nNA= NA=
NA=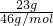 NA=0.5NA,一个二氧化氮分子中含有2个氧原子,
NA=0.5NA,一个二氧化氮分子中含有2个氧原子,
所以23gNO2含有NA个氧原子,故A正确.
B、烧碱的物质的量n=CV=0.1m ol?L-1×1L=0.1mol,一个氢氧化钠化学式中含有一个氢氧根离子,所以1L0.1mol?L-1的烧碱溶液中含有0.1NA个OH-,故B正确.
C、气体摩尔体积只适用于气体,常温常压下,四氯化碳是液体,所以气体摩尔体积不适用于该物质,故C错误.
D、铁与盐酸反应生成氯化亚铁,所以1mol铁与足量的盐酸反应,转移2NA个电子,故D错误.
故选AB.
点评:本题考查了阿伏伽德罗常数的有关计算,难度不大,易错选项是C,注意气体摩尔体积只适用于气体,不适用于固体和液体.
本题难度:一般