1、选择题 乙酸乙酯、甲酸甲酯、乙酸丙酯三种物质组成的混合酯中,若氧元素的质量分数为30%,那么氢元素的质量分数可能是
A.10%
B.20%
C.30%
D.40%
参考答案:A
本题解析:乙酸乙酯、甲酸甲酯、乙酸丙酯三种物质组成通式为(CH2O)n,碳氢比例相同,C:H=6:1(质量比),所以C占 6/7,而碳和氢元素的质量分数为1-30%=70%,其中H元素的质量分数为70%×(1/7)=10%。故选A。
点评:本题难度较大,考查混合物中元素的质量分数的计算,本题解题的关键是利用混合物中各成分的化学式得出C、H的固定组成。
本题难度:一般
2、选择题 现有某天然有机物,拟对其进行研究,一般采取的研究步骤是
A.分离提纯→确定化学式→确定分子式→确定结构式
B.分离提纯→确定实验式→确定分子式→确定结构式
C.分离提纯→确定结构式→确定实验式→确定分子式
D.确定分子式→确定实验式→确定结构式→分离提纯
参考答案:B
本题解析:研究有机物的一般方法是,先分离提纯,再通过元素分析,确定其实验式,然后利用质谱法测定相对分子质量来确定分子式,最后通过光谱分析来确定其结构式。
点评:本题属于简单题,熟悉教材,理解教材,体会科学研究的一般逻辑。
本题难度:一般
3、选择题 某有机物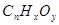 完全燃烧需氧气的物质的量是该有机物的n倍,生成CO2和H2O的物质的量相等。该有机物中n、x、y的关系是:
完全燃烧需氧气的物质的量是该有机物的n倍,生成CO2和H2O的物质的量相等。该有机物中n、x、y的关系是:
A.n==2x==y
B.2n==x==2y
C.n==x==2y
D.2n==x==y
参考答案:B
本题解析:略
本题难度:简单
4、选择题 下列实验中操作、现象、结论对应关系正确的一组是(?)
选项
| 操作
| 现象
| 结论
|
A
| 在蔗糖中加入几滴水搅拌均匀,再加入浓硫酸,迅速搅拌
| 蔗糖逐渐变黑,体积膨胀,形成疏松多孔的物质
| 只体现了浓硫酸的脱水性
|
B
| 淀粉和稀硫酸混合共热后,再加少量新制氢氧化铜悬浊液
| 产生红色沉淀
| 淀粉水解可生成葡萄糖
|
C
| 溴乙烷和氢氧化钠溶液充分反应后,用足量稀硝酸酸化,再加入硝酸银溶液
| 生成淡黄色沉淀
| 溴乙烷中含有溴元素
|
D
| 将溴水加入苯中并充分振荡
| 溴水褪色
| 苯与溴发生了取代反应
参考答案:C
本题解析:A选项表现了浓硫酸的强氧化性和脱水性。故A选项是错误的,B选项能使新制的氢氧化铜溶液产生红色沉淀的,除了葡萄糖还有麦芽糖,因此不能由此断定淀粉水解的产物是葡萄糖。D选项主要是发生了萃取。因此D选项是错误的。
本题难度:一般
5、选择题 下列说法正确的组合是? (? )
①用溴水除去混在苯中的己烯,分液得到纯净的苯
②将电石与水反应产生的乙炔通入溴水中,溴水褪色,证明乙炔和溴水发生了加成反应?
③将溴乙烷和NaOH乙醇溶液混合共热,生成的气体直接通入酸性高锰酸钾溶液,酸性高锰酸钾溶液褪色,说明有乙烯生成
④用淀粉碘化钾试纸和白醋溶液可以检验加碘盐中的碘元素
⑤油脂在NaOH稀溶液中发生水解反应后,若静置不分层,说明水解完全
⑥丙氨酸中有手性碳原子
A.①②③
B.④⑤⑥
C.②③④
D.③④⑤
参考答案:B
本题解析:①己烯能够与溴水发生反应产生卤代烃留在溶液中,但是由于溴单质溶液在苯中溶解,所以用溴水除去混在苯中的己烯,不能分液得到纯净的苯,错误;②由于电石中含有少量的CaS,将电石与水反应产生的乙炔中含有H2S,通入溴水中,溴水褪色,也可能是H2S与溴水发生氧化还原反应的缘故,所以不能证明乙炔和溴水发生了加成反应,错误;③将溴乙烷和NaOH乙醇溶液混合共热,生成的气体直接通入酸性高锰酸钾溶液,酸性高锰酸钾溶液褪色,也可能是挥发出的有还原性的乙醇反应的结果,所以不能说明有乙烯生成,错误;④在加碘盐中碘元素是以KIO3的形式存在的。若用淀粉碘化钾试纸和白醋溶液就会发生氧化还原反应产生I2,可以使试纸变为蓝色,可以检验加碘盐中的碘元素,正确;⑤油脂不能在水中溶解,若在NaOH稀溶液中完全发生水解反应后,产生的甘油和高级脂肪酸的钠盐都在溶解,乙醇不会出现分层现象。故若静置不分层,说明水解完全,正确;⑥在丙氨酸中有一个C原子连接了四个不同的原子或原子团,乙醇有手性碳原子,正确。
本题难度:一般
|