|
|
|
高中化学知识点大全《化学实验的基本操作》高频试题强化练习(2019年最新版)(八)
2019-06-28 21:48:32
【 大 中 小】
|
1、选择题 下列说法中正确的是
A.在饱和硫酸铜溶液中放入胆矾晶体,几天后晶体外形发生改变且晶体质量变小。
B.检验火柴头中的氯元素,可把燃尽的火柴头浸泡在少量水中,片刻后取少量溶液于试管中,滴加硝酸银溶液和稀硝酸
C.做“钠与水的反应”实验时,切取绿豆大小的金属钠,用滤纸吸干其表面的煤油, 放入烧杯中,滴入两滴酚酞溶液,再加入少量水,然后观察并记录实验现象
D.在比较乙醇和苯酚与钠反应的实验中,要把乙醇和苯酚配成同物质的量浓度的水溶液,再与相同大小的金属钠反应,来判断两者羟基上氢的活性
参考答案:B
本题解析:A、在饱和硫酸铜溶液中放入胆矾晶体,晶体形状可能会改变,但质量不变,错误;B、正确;C、应把钠放到水中,错误;D、钠与水反应剧烈,不能比较出结果,错误。
本题难度:简单
2、实验题 (6分)某学生为测定未知浓度的硫酸溶液,以0.1400mol/L的NaOH溶液滴定上述H2SO4,取待测硫酸25.00mL,滴定终止时消耗NaOH溶液15.00mL。
(1)若使用甲基橙做指示剂,如何确定终点?? (2)下列操作将导致测定值高于实际值的是??
A.标准液在“0”刻度线以上,未予调整就开始滴定
B.碱式滴定管用蒸馏水洗涤后未用标准NaOH溶液润洗
C.观察记录滴定管内液面刻度时滴定前仰视,滴定后俯视
D.酸滴定管经蒸馏水洗净后,即注入锥形瓶进行中和滴定
| E.在滴定过程中不慎将数滴酸液滴在锥形瓶外
(3)计算待测硫酸溶液的物质的量浓度为? mol/L(计算出结果到小数点后二位)
参考答案:溶液由红色突然变成黄色且半分钟不恢复原色;B 0.042mol/L
本题解析:(1)甲基橙的变色范围为3.1~4.4,颜色变化为红、橙、黄,当向硫酸溶液中加入甲基橙,溶液颜色为红色,当加入氢氧化钠溶液时,溶液酸性减弱,溶液颜色由红色突然变成黄色且半分钟不恢复原色即达滴定终点;
(2)下列操作将导致测定值高于实际值的是:碱式滴定管用蒸馏水洗涤后未用标准NaOH溶液润洗,导致标准液浓度偏小,滴定硫酸时消耗体积增多,计算出的硫酸浓度偏高;
(3)根据酸碱中和反应的方程式可得,待测硫酸溶液的物质的量浓度为0.042mol/L
本题难度:一般
3、选择题 遇到下列情况,处理不当的是
A.不小心将少量浓硫酸沾到皮肤,立即用水冲洗.
B.皮肤上沾有浓碱溶液时,立即用酒精冲洗.
C.为了避免浪费,应该把实验用剩的药品放回原试剂瓶中.
D.连接并组装成套仪器时,一般按自下而上、从左到右的顺序进行安装.
参考答案:D
本题解析:
本题难度:困难
4、选择题 下列实验操作合理的是
A.用酒精萃取碘水中的碘
B.用托盘天平称取5.20 g氯化钠
C.用100 mL量筒量取5.20 mL盐酸
D.用坩埚灼烧干海带得到海带灰
参考答案:D
本题解析:A、酒精易溶于水,不能做萃取剂,故错;B、托盘天平精确到0.1g,故错;C、量筒精确到0.1mL,故错。故选D。
本题难度:一般
5、实验题 (18分) 三个课外实验小组用Na2SO3溶液、FeCl3溶液及其它试剂做了一系列实验:
第一组:烧瓶中盛装滴有酚酞的 Na2SO3溶液,并放置在盛有水的烧杯中,然后向烧杯中加入浓硫酸,实验过程中发现烧瓶中溶液红色_____(填“变深”、“变浅”或“不变”),下列有关叙述正确的是_________(填字母)。
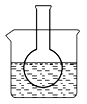
A.溶液显浅红色是因为Na2SO3水解呈酸性
B.水解反应为放热反应
C.水解反应为吸热反应
D.升高温度,Na2SO3水解程度增大
|
第二组:该小组讨论Fe3+和SO32-之间发生怎样的反应,提出了三种假设:①是发生氧化还原反应:2Fe3++SO32-+ H2O = 2Fe2++ SO42-+ 2H+;②是发生双水解反应:2Fe3++ 3SO32-+ 6H2O = 2Fe(OH)3(胶体) + 3H2SO3;③是两种反应同时发生。为了验证假设,同学们进行了下列实验,请填写下列空白:
(1)用试管取适量Na2SO3溶液,加入BaCl2稀溶液,有白色沉淀生成,再加稀盐酸,沉淀全部溶解,然后再进行后续实验。该实验操作的目的是______________________。
(2)取5 mL FeCl3溶液于试管中,逐滴加入Na2SO3溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3溶液至过量,溶液颜色最终变为红褐色。这种红褐色液体是__________________。向红褐色液体中加足量盐酸,将所得溶液分成两份,其中一份加入KSCN溶液,溶液变成血红色,反应的离子方程式为________________________;另一份加入BaCl2稀溶液,产生少量白色沉淀,白色沉淀为________(填化学式)。
(3)由上述实验现象说明假设__________(填编号)是正确的。
第三组:用0.1000mol/L的酸性KMnO4溶液滴定未知浓度的Na2SO3溶液,用碱式滴定管量取25.00mL Na2SO3溶液于锥形瓶,用_____式滴定管盛装KMnO4溶液进行滴定,滴定终点颜色变化为:_____色变为_____色;重复三次实验,测得消耗的KMnO4溶液体积平均值为20.00mL,则Na2SO3的浓度为____________mol/L。
参考答案:(共18分)
第一组:?变深?(1分)?
C D? (2分)
第二组:(1)检验Na2SO3溶液是否变质?(2分)
(2)Fe(OH)3胶体? (1分)
Fe3+ + 3SCN-?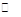 ?Fe(SCN)3?(2分)
?Fe(SCN)3?(2分)
BaSO4?(2分)
(3)③? (2分)
第三组:酸? (1分)
无色变为紫(红)色? (2分)
0.2000 mol/L?(3分)
本题解析:第一组:盐类的水解为吸热反应:SO32-+H2O HSO3-+OH-;浓硫酸与水混合放出大量的热,促进了Na2SO3的水解,溶液碱性增强,红色加深:
HSO3-+OH-;浓硫酸与水混合放出大量的热,促进了Na2SO3的水解,溶液碱性增强,红色加深:
第二组:(1)Na2SO3易被氧化为Na2SO4,必须先检验其是否变质,否则将影响下面的SO42-的检测
(2)Fe(OH)3(胶体)为红褐色;
铁离子与SCN―可生成络合物呈血红色:Fe3+ + 3SCN- Fe(SCN)3
Fe(SCN)3
不溶于酸的白色沉淀,一定为BaSO4;
(3)综合上面的实验事实可知,两物质同进发生了两种反应,故选③
第三组:KMnO4溶液具有强氧化性,可腐蚀橡胶管,故只能用酸式滴定管最取;
KMnO4溶液本身具有紫色,当滴下一滴液体,紫色不褪去,并且半分钟不褪,则视为滴定终点;
由反应:2MnO4―~5SO32―可知,KMnO4的物质的量为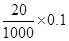 mol=0.002mol,SO32―的物质的量为0.005mol,Na2SO3的浓度为
mol=0.002mol,SO32―的物质的量为0.005mol,Na2SO3的浓度为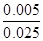 =0.2000 mol/L
=0.2000 mol/L
本题难度:简单
 ?Fe(SCN)3?(2分)
?Fe(SCN)3?(2分) HSO3-+OH-;浓硫酸与水混合放出大量的热,促进了Na2SO3的水解,溶液碱性增强,红色加深:
HSO3-+OH-;浓硫酸与水混合放出大量的热,促进了Na2SO3的水解,溶液碱性增强,红色加深: Fe(SCN)3
Fe(SCN)3 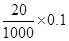 mol=0.002mol,SO32―的物质的量为0.005mol,Na2SO3的浓度为
mol=0.002mol,SO32―的物质的量为0.005mol,Na2SO3的浓度为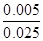 =0.2000 mol/L
=0.2000 mol/L