1、填空题 (12分)下表是元素周期表的一部分,列出了七种元素的周期表中的位置:
?
| ⅠA
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅦA
|
2
| ?
| ?
| ?
| ①
| ?
| ②
| ③
|
3
| ④
| ⑤
| ⑥
| ?
| ?
| ?
| ⑦
|
请用化学符号按要求回答下列问题:
(1)这七种元素中,非金属性最强的是??,在元素周期表中的位置?
(2)元素①与②形成摩尔质量为44g /mol的物质,它的电子式是?
(3)③、⑥、⑦三种元素的原子半径由大到小的顺序是?。
(4)④元素最高价氧化物对应的水化物与⑥元素的最高价氧化物对应的水化物反应的化学反应方程式是?
(5)④、⑤、⑥三种元素最高价氧化物的水化物碱性强弱顺序是?
参考答案:(1)F?第2周期ⅦA(2)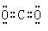 (3)Al>Cl>F
(3)Al>Cl>F
(4)NaOH+ Al(OH)3?Na[Al (OH)4](5)NaOH> Mg(OH)2> Al(OH)3
本题解析:考查元素周期表的结构和元素周期律的应用。根据元素在周期表中的位置可知①是C,②是O,③是F,④Na,⑤是Mg,⑥是Al,⑦是Cl。
(1)同周期元素自左向右金属性之间减弱,非金属性逐渐增强。同主族元素自上而下金属性逐渐增强,非金属性逐渐减弱。
(2)元素①与②形成摩尔质量为44g /mol的物质是CO2,含有极性键。
(3)同周期元素自左向右原子半径逐渐减小,同主族元素自上而下原子半径逐渐增大。
(4)④元素最高价氧化物对应的水化物与⑥元素的最高价氧化物对应的水化物分别是氢氧化钠和氢氧化铝,氢氧化铝是两性氢氧化物,可溶于强碱。
本题难度:一般
2、填空题 已知X、Y、Z、W是短周期内的四种非金属元素,它们的原子序数依次增大。X元素原子形成的离子就是一个质子,Y、Z在元素周期表中处于相邻位置,它们的单质在常温下均为无色气体,W元素的最高正价与最低负价的代数和为4。
(1)请写出元素符号W?;
(2)W单质与Z单质的反应产物在一定条件下与Z单质反应,该反应的化学方程式:?。
(3)这四种元素组成原子个数比为:8:2:4:1的化合物,该化合物的化学式为?。
(4)Y元素的最高价氧化物对应的水化物与Y元素的氢化物可以反应,写出该反应的的化学方程式?。
参考答案:1)S;?(2)2SO2+O2? 2SO3
(3)(NH4)2SO4?(4)NH3+HNO3==NH4NH3
本题解析:略
本题难度:简单
3、选择题 一次区分乙酸、乙醇、苯、四氯化碳四种液体的试剂是
A.H2O
B.溴水
C.新制Cu(OH)2
D.酸性高锰酸钾溶液
参考答案:C
本题解析:根据与水的互溶性及密度大小,可知乙酸、乙醇与水互溶,可通过新制新制Cu(OH)2鉴别;而苯与水分层,且油层在上方,四氯化碳与水分层,且没层在下方;
本题难度:简单
4、填空题 A、B、C、D、E、F为原子序数依次增大的六种元素。已知:A是周期表中原
子半径最小的元素.B的基态原子核外电子有 7种运动状态,B、C、E三种元素原子中未
成对电子数之比为3:2:1,D原子核外有4个能级且均充满电子,D与E可形成DE2型化
合物,F原子核外最外层只有1个电子,其余各层均充满电子。
回答下列问题:
(1)写出下列元素的名称:B??C???E ?
(2)F在周期表位位于?区,与F同周期且未成对电子数最多的元素为?(填
写元素符号),该元素价电子排布图为?;
(3)B与D组成的化合物可以与水反应,写出它与水反应的化学方程式?
参考答案:(1)氮、氧、氯;
(2)ds;Cr;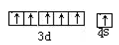 ;
;
(3)Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
本题解析:A、B、C、D、E、F为原子序数依次增大的六种元素,由A是周期表中原子半径最小的元素可推出A是氢元素,B的基态原子核外电子有 7种运动状态,可知B是氮元素,B、C、E三种元素原子中未成对电子数之比为3:2:1,可推出C是氧元素,由于D原子核外有4个能级且均充满电子,D与E可形成DE2型化
合物,可推出E是氯元素,D是镁,再由F原子核外最外层只有1个电子,其余各层均充满电子,可推出F为铜元素,与F同周期且未成对电子数最多的元素为Cr,该元素价电子排布图为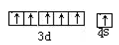 ,B与D组成的化合物与水反应的化学方程式为)Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
,B与D组成的化合物与水反应的化学方程式为)Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
回答下列问题:
点评:主要考查元素周期表,历年高考的必考题型,难度不大,解题的关键是要认真审读,挖掘题干隐含的信息,如“原子序数依次增大”,结合原子结构,电子的排布,快速作答。
本题难度:一般
5、选择题 甲~辛等元素在周期表中的相对位置如下表。甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素。下列判断正确的是(?)
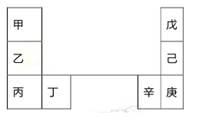
A.金属性:甲>乙>丁
B.原子半径:辛>己>戊
C.丙和庚的原子核外电子数相差13
D.乙的单质在空气中燃烧生成只含离子键的化合物
参考答案:BC
本题解析:戊的一种单质是自然界硬度最大的物质,所以戊是C元素;则己、庚分别是Si、Ge元素;甲和戊的原子序数相差3,所以甲是Li元素,则乙、丙分别是Na、K元素;则丁是Ca元素,辛是Ga元素。A、根据元素周期律,同主族元素的金属性从上到下逐渐增强,所以金属性:甲<乙<丙,错误;B、电子层数越多,原子半径越大,所以原子半径:辛>己>戊,正确;C、丙的原子序数是19,庚的原子序数是32,所以原子的核外电子数的差值也即原子序数的差值,丙与庚的原子核外电子数相差13,正确;D、Na在空气中燃烧生成过氧化钠,既含离子键又含共价键,错误,答案选BC。
本题难度:一般