1��ѡ���� ��֪�����ӵ�������ֵΪNA��������˵����ȷ����
A.1?mol/L?CuCl2��Һ�к��е�Cl-�ĸ���Ϊ2NA
B.14?g?CnH2n�к��еĹ��õ��Ӷ���ΪNA
C.���³�ѹ��46?gNO2��N2O4�Ļ�������к��е�ԭ����Ϊ3NA
D.4.6?g?Na������������ȫ��Ӧ����Na2O��Na2O2�Ļ�����к��е�������������O.1NA
�ο��𰸣�C
���������������A���Ȼ�ͭ��Һ�������֪���������Ȼ�ͭ�����ʵ�����
B��14 g CnH2n�к���0.1molCH2�����õ��Ӷ���һ������0.1mol��
C��46 gNO2��N2O4�Ļ���������൱�ں���1molNO2������3molԭ�ӣ�
D���Ƶ����ʵ�����0.2mol����Ӧ������0.1molNa2O��Na2O2�Ļ���������Ϊ0.1mol��
���A������û�и����Ȼ�ͭ��Һ�����ʵ���������������Һ�������ӵĸ�������A����
B��CnH2n�ķ����к���̼�⡢̼̼���õ��Ӷԣ��� 14 g CnH2n�к��еĹ��õ��Ӷ�������NA����B����
C������46 gNO2��N2O4�Ļ�����������ɿ��Կ��ɺ���1molNO2���ʺ��е�ԭ����Ϊ3NA����C��ȷ��
D��������ԭ���غ㣬4.6g����0.2mol��������0.1molNa2O��Na2O2�Ļ���������Ϊ0.1mol����D����
��ѡC��
���������⿼�鰢��٤��������ע����Һ��Ũ�Ⱥ���������ߣ����ܼ������ʵ����ʵ����������Ѷ��еȣ�
�����Ѷȣ���
2��ѡ���� ���������У�����������Ĵ�С��ϵ�������
A.����ķ�����
B.�¶�
C.ѹǿ
D.���Ӵ�С
�ο��𰸣�D
���������������Ӱ���������������������Ŀ�����ӱ�����С�Լ����Ӽ�ľ��룮�¶ȡ�ѹǿ����������Ӽ�࣮
���Ӱ���������������������Ŀ�����ӱ�����С�Լ����Ӽ�ľ�������أ��¶ȡ�ѹǿ����������Ӽ�࣮����������˵��������Ӽ�ľ���Զ���ڷ��ӱ����Ĵ�С�����ӱ������Ժ��Բ��ƣ�
��ѡ��D��
���������⿼��Ӱ���������������С�����أ���Ŀ�ѶȲ���ע����ͬ��ͬѹ�£�������Ӽ��ƽ��������ȣ�������������أ�Ӱ�����������������Ҫ����������ķ�������
�����Ѷȣ���
3��ѡ���� ��H2��O2��CO2��ɵĻ��������ܶ���ͬ��ͬѹ��CH4�ܶȵ�2��������������ֵ����ʵ���֮�Ȳ�������
A.2 ��3 ��5
B.2 ��5 ��5
C.2 ��1 ��5
D.2 ��2 ��7
�ο��𰸣�D
�����������������ƽ��ʽ��Ϊ16��2=32�������������������ʽ��ǡ��ҲΪ32��ֻ��ҪH2��CO2��ƽ��ʽ��Ϊ32���ɣ���ʮ�ֽ��淨��֪���ߵ����ʵ���֮��Ϊ2��5�����Դ�ΪD
�����Ѷȣ���
4��ѡ���� NA��ʾ�����ӵ�������������������ȷ����
A.��״����2.24L���ȼ��麬�з�����ĿΪ0.1NA
B.��״����1.8?g?H2O���з�����ĿΪ0.1NA
C.3.2?g����ͭ��ַ�Ӧ������ת������Ϊ0.1NA
D.�����£�100mL?lmol/L��Na2CO3��Һ�е���������Ŀ����0.1NA
�ο��𰸣�BD
���������������A����״�����ȼ��鲻�����壻
B������n=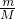 =
=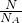 ������õ���������
������õ���������
C�����ͭ��Ӧ��������ͭ������n=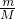 �����������ԭ��Ӧ�������ת�ƣ�
�����������ԭ��Ӧ�������ת�ƣ�
D��ˮ��Һ��̼�������ˮ�⣻
���A����״�������ȼ��鲻�����壬2.24L���ȼ��鲻��0.1mol�����з�����Ŀ����0.1NA����A����
B��1.8 g H2O���ʵ���Ϊ0.1mol�����з�����ĿΪ0.1NA����B��ȷ��
C��3.2 g�����ʵ���Ϊ0.1mol����ͭ��ַ�Ӧ��2Cu+S=Cu2S��S��Cu2S��2e-������ת������Ϊ0.2NA����C����
D�������£�100mL lmol/L��Na2CO3��Һ��̼����������ʵ���0.1mol��̼�������ˮ�⣬CO32-+H2O?HCO3-+OH-����Һ�е���������Ŀ����0.1NA����D��ȷ��
��ѡBD��
���������⿼���˰���٤��������Ӧ�ã���Ҫ��������Ħ�����������Ӧ�ã�����ˮ��ķ�����������ԭ��Ӧ�ĵ���ת�Ƽ��㣬ע��̼�������ˮ�����������࣬��Ŀ�Ѷ��еȣ�
�����Ѷȣ�һ��
5��ѡ���� ͬ��ͬѹ�£���������SO2��CO2��Ƚϣ�������������ȷ����
A.�ܶȱ�Ϊ1��1��
B.�ܶȱ�Ϊ11��16��
C.�����Ϊ11��16����
D.�����Ϊ16��11
�ο��𰸣�C
���������ͬ��ͬѹ�£�������ܶ�֮���������Ħ������֮�ȣ�����SO2��CO2���ܶ�֮����64�U44��16�U11��A��B������ȷ����������ȵ������£���������֮���������Ħ������֮�ȵķ��ȣ���44�U64��11�U16��C��ȷ��D����ȷ����ѡC��
�����Ѷȣ���