1��ѡ���� ���з���������ԭ�Ӷ����������8���ӽṹ���ǣ�������
A��������COCl2��
B����������
C�����Ȼ���
D����������
�ο��𰸣�A��������COCl2����CԪ�ػ��ϼ�Ϊ+4��Cԭ������������Ϊ4������4+4=8��Cԭ�ӣ�����8���ӽṹ��OԪ�ػ��ϼ�Ϊ-2�ۣ�Oԭ������������Ϊ6������2+6=8��Oԭ������8���ӽṹ��ClԪ�ػ��ϼ�Ϊ-1��Clԭ������������Ϊ7������1+7=8��Clԭ������8���ӽṹ����A��ȷ��
B������������SԪ�ػ��ϼ�Ϊ+6��Sԭ������������Ϊ6������6+6=12��Sԭ�Ӳ�����8���ӽṹ��FԪ�ػ��ϼ�Ϊ-1��Fԭ������������Ϊ7������1+7=2��Fԭ������8���ӽṹ����B����
C��PCl3��PԪ�ػ��ϼ�Ϊ+3��Pԭ������������Ϊ5������3+5=8��Pԭ������8���ӽṹ��ClԪ�ػ��ϼ�Ϊ-1��Clԭ������������Ϊ7������1+7=8��Clԭ������8���ӽṹ����C��ȷ��
D��BF3��BԪ�ػ��ϼ�Ϊ+3��Bԭ������������Ϊ3������3+3=6��Bԭ�Ӳ�����8���ӽṹ��FԪ�ػ��ϼ�Ϊ-1��Fԭ������������Ϊ7������1+7=8��Fԭ������8���ӽṹ����D����
��ѡAC��
���������
�����Ѷȣ�һ��
2��ѡ���� ��bXn+��aYm-�����ӣ����Ǿ�����ͬ�ĵ��Ӳ�ṹ����a��m��n��b�Ĺ�ϵΪ��������
A��a=b-m-n
B��a=b+m+n
C��a=b-m+n
D��a=m-n+b
�ο��𰸣������Ӻ��������=������-���������������bXn+�ĺ��������Ϊb-n��
�����Ӻ��������=������+�����ĵ����������aYm-�ĺ��������Ϊa+m��
bXn+��aYm-�����Ӿ�����ͬ�ĵ��Ӳ�ṹ��˵�����ߺ����������ͬ������b-n=a+m����a=b-m-n��
��ѡ��A��
���������
�����Ѷȣ���
3��ѡ���� ����ѡ�⣩�����л�ѧ������ȷ���ǣ�������
A��N2�Ľṹʽ��N��N
B���Ҵ�������������ǵ����ʽ��Ϊ��CH2O
C��������ӵ����ģ�ͣ�
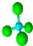
D��Sԭ�ӵĵ����Ų�ʽ��1s22s22p63s23p4
�ο��𰸣�AD
���������
�����Ѷȣ�һ��
4��ѡ���� ���ڣ���ѧ����NaNO3��Na2O��573K�·�Ӧ�Ƶ������ӻ�����NaxNO4�����ⶨ����NO4x-�еĸ�ԭ�ӵ��������Ӷ��ﵽ��8�������ȶ��ṹ����xΪ��������
A��1
B��2
C��3
D��4
�ο��𰸣�NO4x-�и�ԭ���������Ӷ��ﵽ8���ӽṹ����32�����ӣ���һ��Nԭ�Ӻ�4��Oԭ������㹲�У�5+4��6=29�������ӣ��ʻ���õ�3�����ӣ����x=3��
��ѡC��
���������
�����Ѷȣ���
5������� A��B��C��D�Ƕ�������ԭ�������������������Ԫ�أ���֪Cԭ�������������Ǵ�����������1/2��B�ĺ˵������A��2����Dԭ�Ӻ��е���������B��3����1mol����A������ȫ��Ӧʱ������1g������
д������1��Cԭ�ӽṹʾ��ͼ______������Ԫ�����ڱ��е�λ����______��
��2��AԪ�ص�����������Ӧˮ����ĵ���ʽ______��
��3���õ���ʽ��ʾDԪ���γ���̬�⻯��Ĺ��̣�
______
��4��A��D��Ԫ�ص�����������Ӧˮ����ֱ���B������������Ӧˮ���ﷴӦ�����ӷ���ʽ��______��
�ο��𰸣���1��CΪ��Ԫ�أ�ԭ�ӽṹʾ��ͼΪ ����Ԫ�����ڱ��е�λ���ǵ������ڡ��ڢ�A�壬�ʴ�Ϊ��
����Ԫ�����ڱ��е�λ���ǵ������ڡ��ڢ�A�壬�ʴ�Ϊ�� ���������ڡ��ڢ�A�壻
���������ڡ��ڢ�A�壻
��2��NaOH�������Ӻ�����������֮��������Ӽ�����ԭ�Ӻ���ԭ��֮����ڹ��ۼ����������������м������Ӽ����й��ۼ���NaOHΪ���ӻ���������ʽΪ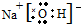 ���ʴ�Ϊ��
���ʴ�Ϊ��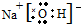 ��
��
��3���������ʽ��ԭ�Ӻ���ԭ�Ӽ�ͨ�����ۼ��γɵĹ��ۻ�������γɹ���Ϊ ��
��
�ʴ�Ϊ�� ��
��
��4��A��D��Ԫ�ص�����������Ӧˮ����ֱ�Ϊ�������ƺ����ᣬBΪ������Ԫ�ص�����ϼ�Ϊ+3������������ﻯѧʽΪAl2O3������������Ӧˮ����ΪAl��OH��3��Al��OH��3���������Ʒ�Ӧ�����ӷ���ʽΪAl��OH��3+OH-�TAlO2-+2H2O��Al��OH��3�����ᷴӦ�����ӷ���ʽΪAl��OH��3+3H+=Al3++3H2O��
�ʴ�Ϊ��Al��OH��3+OH-=AlO2-+2H2O��Al��OH��3+3H+=Al3++3H2O��
���������
�����Ѷȣ�һ��