1、选择题 下列物质中,含有离子键的是
[? ]
A.O3
B.H2O
C.Na2SO4
D.C2H5OH
参考答案:C
本题解析:
本题难度:简单
2、选择题 下列用电子式表示的形成过程正确的是
A.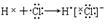
B.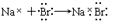
C.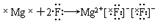
D.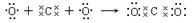
参考答案:D
本题解析:氯化氢是共价化合物,应该是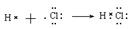 。溴化钠是离子化合物,应该是
。溴化钠是离子化合物,应该是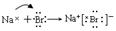 。氟化镁中氟离子的是不能合并的,正确的应该是
。氟化镁中氟离子的是不能合并的,正确的应该是
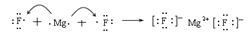 。答案选D。
。答案选D。
本题难度:简单
3、选择题 下列化合物中只含有离子键的是( )
A.NaOH
B.H2O
C.MgO
D.H2SO4
参考答案:C
本题解析:
本题难度:简单
4、简答题 元素周期表是20世纪科学技术发展的重要理论依据之一,是我们学习化学的重要工具.假设NH4+是“元素”NH4的阳离子,则“元素”NH4在周期表中的位置应该是第______周期第______族;“元素”NH4的单质常温常压下应为______(填“固”、“液”或“气”)体;熔点______(填“高”或“低”);______(填“能”或“不能”)导电;NH4的碳酸盐应______(填“易”或“不易”)溶于水.
参考答案:“元素”NH4的质子数为7+1×4=11,与Na的质子数相同,则应在第三周期第IA族,
钠为固体,熔点低,能导电,碳酸钠易溶于水,
由性质的相似性可知,
则“元素”NH4的单质常温常压下为固体,熔点低,能导电,NH4的碳酸盐易溶于水,
故答案为:三;IA;固;低;能;易.
本题解析:
本题难度:一般
5、选择题 三氟化硼(BF3)是一种无色气体,用于制造火箭的高能燃料。已知BF3是非极性分子,下列描述正确的是
A.BF3分子呈三角锥形
B.BF3沸点低于BCl3
C.B-F键键能低于B-Cl键
D.F-B-F间的夹角为109°28′
参考答案:B
本题解析:A、BF3分子呈平面正三角形,错误;B、BF3相对分子质量小于BCl3,分子间作用力小,溶沸点低,正确;C、F半径小,键长短,B-F键键能高于B-Cl键,错误;D、F-B-F间的夹角为120°,错误。
本题难度:一般