1、选择题 化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是
A.无论是风力发电还是潮汐发电,都是将化学能转化为电能
B.光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅
C.推广燃煤脱硫技术,可以防治SO2污染
D.凡含有食品添加剂的食物对人体健康均有害,不宜食用
参考答案:C
本题解析:A选项是不是化学能转化为电能,而是机械能转化为电能,B选项,制造光缆的主要材料是二氧化硅D选项太绝对了,适量的食品添加剂对人体没有危害。C选项正确,初步开采的煤中含有硫,燃烧可以和氧气反应生成二氧化硫污染空气,脱硫后可以防治二氧化硫污染
本题难度:一般
2、选择题 下列叙述正确的是
[? ]
A.高温下二氧化硅与碳酸钠反应放出二氧化碳,说明硅酸(H2SiO3)的酸性比碳酸强
B.陶瓷、玻璃、水泥容器都能贮存氢氟酸
C.石灰抹墙、水泥砌墙的硬化过程原理相同
D.玻璃窑中出来的气体的主要成分是二氧化碳
参考答案:D
本题解析:
本题难度:简单
3、填空题 (7分)海水是人类宝贵的自然资源,从海水中可以提取多种化工原料。下图是某工厂对海水资源综合利用的示意图。
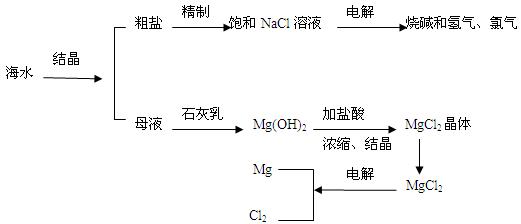
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制后可得NaCl饱和溶液。精制时通常向精盐溶液中依次加入过量的BaCl2溶液,过量的NaOH溶液和过量的Na2CO3溶液,过滤出沉淀后再向滤液加入盐酸至溶液呈中性。请写出下列操作中有关化学反应的离子方程式:
①向溶液中加入过量的Na2CO3溶液:__________________、_____________________;
②电解氯化钠溶液:______________________________________________。
(2)母液中含有K+、Na+、Mg2+等阳离子,从图中可以看出,对母液进行一系列的加工可制得金属镁。
①从离子反应的角度思考,在母液中加入石灰乳所起的作用是:(用离子反应方程式回答)___________________________。
②简述怎样操作才能由氯化镁晶体得到无水氯化镁:____________________________。
参考答案:(7分)
(1)?①Ba2+ + CO32-="=" BaCO3↓、? Ca2+ + CO32-="=" CaCO3↓(共2分)
②2Cl-+2H2O 2OH-+H2↑+Cl2↑(2分)
2OH-+H2↑+Cl2↑(2分)
(2) ①Ca(OH)2+Mg2+==Mg(OH)2+Ca2+? (2分)
②?在HCl气体氛围下加热? (1分)
本题解析:略
本题难度:一般
4、选择题 冶炼金属一般有下列四种方法:①焦炭法;②水煤气(或氢气,或一氧化碳)法;③活泼金属置换法;④电解法。四种方法在工业上均有应用。古代有(I)火烧孔雀石炼铜;(Ⅱ)湿法炼铜;现代有(Ⅲ)铝热法炼铁;(Ⅳ)从氯化镁中炼镁,对它们的冶炼方法的分析不正确的是(?)
A.(I)用①
B.(Ⅱ)用②
C.(Ⅲ)用③
D.(Ⅳ)用④
参考答案:B
本题解析:(Ⅱ)湿法炼铜是在溶液中置换出铜。
本题难度:一般
5、填空题 在元素周期表中,铝在硼的正下方,它们有很多相似的化学性质,可以形成许多组成和性质类似的化合物。单质硼可以通过硼镁矿Mg2B2O5・H2O来制取。
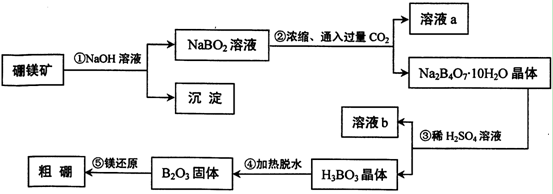
(1)写出步骤①的化学方程式?,
(2)写出步骤②的离子方程式?,
(3)写出表示溶液a物料守恒的关系?;
(4)步骤③中加入稀H2SO4的作用是?;
(5)将制得的粗硼在一定条件下反应全部生成BI3,BI3热分解可以得到纯净的单质硼。0.25 g粗硼制成的BI3分解得到的I2全部被收集后,用2.00 mol/L Na2S2O3溶液滴定,达到滴定终点时消耗27.00 mL Na2S2O3溶液。(已知:I2+2S2O32-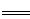 2I-+S4O62-)
2I-+S4O62-)
①滴定过程中所用的指示剂为?,滴来源:91考试网 91Exam.org定终点的现象是?;
②粗硼中硼的含量为____?;
(6)利用硼砂晶体(Na2B4O7?10H2O)可制备过硼酸钠,它是一种优良的漂白剂,被广泛应用于洗衣粉、漂白粉、洗涤剂中。已知纯净的过硼酸钠晶体中各元素的物质的量之比为以n(Na):n(B):n(H):n(O)=1:1:n:7。取过硼酸钠晶体在70℃以上加热将逐步失去结晶水,测得固体质量随温度的变化如图所示,则乃时所得晶体的化学式为?,请写出简要的解题过程。
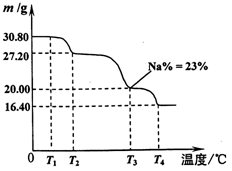
参考答案:(1)Mg2B2O5・H2O+2NaOH = 2NaBO2+2Mg(OH)2↓(2分)
(2)2Na++4BO2-+2CO2+11H2O =?Na2B4O7・10H2O↓+2HCO3-(2分)
(3)c(Na+) = c(CO32-) + c(HCO3-) + c(H2CO3) (2分)
(4)利用强酸制备弱酸H3BO3 (1分)
(5)①淀粉溶液(1分)?溶液由蓝色恰好变为无色(1分)
②79.2%(2分)
(6)NaBO3・H2O(1分)?
解题过程?(3分)
解:T3时? n(Na)=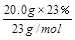 =" 0.2" mol?(1分)
=" 0.2" mol?(1分)
则30.80 g样品中,依n(Na)∶ n(B)∶n(H)∶n(O)=l∶1∶n∶7可得
0.2 mol × 23 g/mol + 0.2 mol × 11 g/mol + 0.2n × 1g/mol + 7 × 0.2 mol × 16 g/mol =" 30.80" g
解得n = 8
故原晶体为NaBO3・4H2O?(1分)
设T3时晶体的化学式为NaBO3・mH2O
则由T3时晶体中钠元素的质量分数可得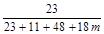 ?× 100% = 23%
?× 100% = 23%
解得m = 1
所以T3时晶体的化学式为NaBO3・H2O(1分)
本题解析:(3)通入过量二氧化碳得到的是碳酸氢钠溶液,所以有c(Na+) = c(CO32-) + c(HCO3-) + c(H2CO3) 。
(5)①Na2S2O3溶液成碱性,S2O32-离子水解溶液显示碱性,反应的离子方程式为:S2O32-+H2O?HS2O3-+OH-;滴定过程中有碘单质参与,可以使用淀粉溶液作为指示剂;滴定结束时,锥形瓶中溶液蓝色褪去且30s内不褪色。
②硫代硫酸钠的物质的量为:2.00mol/L×0.027L=0.054mol,根据关系式:B~BI3~3/2I2~3S2O32-,n(B)=1/3n(S2O32-)=0.018mol,硼的质量为:11g/mol×0.018mol=0.1944g,粗硼中硼的含量为: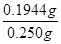 ×100%=79.2%,故答案为:79.2%;
×100%=79.2%,故答案为:79.2%;
本题难度:一般