1、计算题 为测定一种气态烃A的分子式,取一定量的A置于密闭容器中燃烧,定性实验表明产物是CO2、CO、水蒸气。学生甲、乙设计了如下两个方案,均认为根据自己的方案能求出A的实验式。他们测得的有关数据如下(图中的箭头表示气体的流向,实验前系统内的空气已排除)。试完成下列问题:
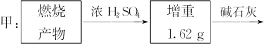
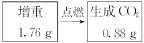
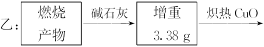

(1)两种方案能否都可求出A的实验式(即C、H原子数比)?
(2)若能求,通过计算求出A的实验式。
(3)若要确定A的分子式,是否还需要测定其他数据?如果需要,该测定哪些数据?
参考答案:(1)甲方案可以
(2)CH3
(3)需要测定A的密度(标准状况)(或A的摩尔质量)
本题解析:欲测A的实验式,需测知C、H两元素的物质的量之比,即需测知:CO与CO2、H2O的物质的量,甲方案可达此要求,
而乙方案将燃烧产物通过碱石灰时,H2O和CO2一同被吸收,测出的数据为CO2和H2O的质量和,故不能。
本题难度:简单
2、填空题 下列物质:①O2 ②三氯甲烷 ③CH3CH2CH2OH? ④O3 ⑤CHCl3 ⑥CH3OCH2CH3
⑦C? ⑧CH3CH(OH)CH3 ⑨C ⑩CH3OH。其中属于同系物的有________(填序号,下同),互为同分异构体的有________,互为同素异形体的有________,属于同位素的有________,是同一种物质的有________。
参考答案:③⑩或⑧⑩ ③⑥⑧ ①④ ⑦⑨ ②⑤
本题解析:“四同”的概念及其对象
同位素?质子数相同?中子数不同?同元素原子
同素异形体?同元素结构不同?单质
同系物?结构相似组差n个CH2?化合物
同分异构体?分子式相同结构不同?化合物
点评:“四同”的概念及其对象
同位素?质子数相同 ?中子数不同?同元素原子
同素异形体?同元素结构不同 ?单质
同系物?结构相似组差n个CH2?化合物
同分异构体?分子式相同结构不同 ?化合物
1.同位素与同素异形体
常见同位素: 氕氘氚? /?氧16 氧17 氧18? / 碳12 碳13
同位素的特点: 属于同一原子 同一元素?化学性质相同但物理性质有所不同
常见同素异形体: 金刚石-石墨?红磷-白磷? O2-O3? C60-C70
2.同系物
同系物的性质: 随碳原子个数增加 熔沸点升高?且同系物化学性质相似
同系物的判断: “两同一差”原则?即同通式同结构组差n个CH2
互为同系物的五大结论:1)必符合同一通式? 2)必为同类物质? 3)组成元素相同? 4)结构相似但不一定相同? 5)分子式不同?
3.同分异构体
“五同一异”原则: 同分子式同最简式同元素同相对原子式量同质量分数 结构不同
确定有机物的同分异构体数目:?
1) 等效氢法
烃的一取代物数目的确定,实质上是看处于不同位置的氢原子数目。可用“等效氢法”判断。判断“等效氢”的三条原则是:
① 同一碳原子上的氢原子是等效的;如甲烷中的4个氢原子等同。
② 同一碳原子上所连的甲基是等效的;如新戊烷中的4个甲基上的12个氢原子等同。
③ 处于对称位置上的氢原子是等效的。
注意:在确定同分异构体之前,要先找出对称面,判断等效氢,从而确定同分异构体数目
2)对称轴法
对于多个苯环并在一起的稠环芳烃,要确定两者是否为同分异构体,则可画一根对称轴,再通过平移或翻转来判断是否互为同分异构体。
3)定一移二法
对于二元取代物的同分异构体的判断,可固定一个取代基位置,再移动另一取代基位置以
确定同分异构体数目。
同分异构体的书写技巧:
1)基本方法(对于链烃): 先直链后支链 然后每次把主链碳原子数减一个来作支链
注意: 对称位置不重复?支链不加两端?支链由少到多?两个支链的关系有邻―间―对
2)甲基移位法(对于烃的衍生物):先将官能团至于一端逐个逐位的将甲基从一端向另一端移动。
本题难度:一般
3、选择题 下列化合物的一氯代物的数目排列顺序正确的是(?)
①CH3CH2CH2CH2CH2CH3?②(CH3)2CHCH(CH3)2
③(CH3)3CCH2CH3?④(CH3)3CC(CH3)3
A.①>②>③>④
B.②>③=①>④
C.③>②>④>①
D.①=③>②>④
参考答案:D
本题解析:①中有三种等效氢原子,故其一氯代物有3种;②中有2种等效氢原子,故其一氯代物有2种;
③中有3种等效氢原子,故其一氯代物有3种;④中只有有1种等效氢原子,故其一氯代物有1种。因此,D选项符合题意。
点评:本题考查学生对烷烃一氯代物的同分异构体认识,烷烃中有几种等效氢原子就有几种一氯代物,对等效氢的掌握是解题关键。
本题难度:简单
4、选择题 在下列有关说法中正确的是
①相同质量的CH4、C2H4、C2H2完全燃烧时耗O2量的关系为CH4 > C2H4 >C2H2
②对于任意比混合的乙烯、丙烯和环丁烷混合气体在足量氧气中燃烧,只要混合气体的质量不变,完全燃烧后产生的CO2和H2O的量也不改变
③对于任意比混合的C2H4、C2H6、C2H2混合气体,只要混合气体物质的量不变,完全燃烧后产生的CO2物质的量也不改变
④某有机物在足量氧气中燃烧后产生CO2与H2O的物质的量之比为2:3,则该有机物的类型肯定为烷烃
A.①②③
B.①②③④
C.②③
D.以上组合均不正确
参考答案:A
本题解析:①正确,相同质量的烃,含H量越高耗氧量越多;②正确,乙烯、丙烯的最简式相同,所以只要混合气体的质量不变,完全燃烧后产生的CO2和H2O的量也不改变;③正确,C2H4、C2H6、C2H2混合气体中均有2个碳原子,只要混合气体物质的量不变,完全燃烧后产生的CO2物质的量也不改变;④错,完全燃烧生成二氧化碳气体和水的有机物不一定是烃,也可以是烃的含氧衍生物;
本题难度:一般
5、填空题
合成有机物G(C9H10O2)的过程如下,试回答下列有关问题。
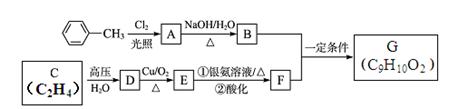
(1)A的分子式为?。
(2)C中的官能团的名称是?;C转化为D的反应类型?。
(3)E转化为F的过程中酸化的目的是?。
(4)写出G与足量NaOH溶液反应的化学方程式:?。
(5)符合下列条件的G的同分异构体数目为?种:
①苯环上有3个取代基,且有两个取代基相同;
②能够与新制的银氨溶液反应产生光亮的银镜。其中氢原子共有四种不同环境的所有物质的结构简式为?、?。
参考答案:
C7H7Cl
(2)碳碳双键?加成反应
(3)使生产的乙酸铵转化为乙酸

本题解析:甲基苯与氯气在光照条件下会发生取代反应,所以A得分子式为C7H7Cl(2)C物质是乙烯所以它的官能团是碳碳双键,碳碳双键主要发生加成反应,所以D物质是乙醇,E物质为乙醛 F为乙酸,加入酸的目的主要是使在银镜反应中生成的乙酸铵转化为乙酸 A物质为一氯甲基苯,卤代烃在氢氧化钠水溶液中发生的是取代反应生成对应的醇所以B为 G为
G为
本题难度:一般