| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点归纳《原电池原理》练习题(八)
参考答案: 本题解析: 本题难度:简单 3、选择题 如图为番茄电池,下列说法正确的是( ) |
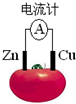
参考答案:A、该原电池中,锌作负极,负极上锌失电子生成锌离子进入溶液,所以锌片的质量会变小,故A正确;
B、铜作正极,正极上氢离子得电子生成氢气,所以铜电极附近不会出现蓝色,故B错误;
C、锌作负极,铜作正极,电子从锌沿导线流向铜,故C错误;
D、锌作该原电池的负极,故D错误;
故选A.
本题解析:
本题难度:一般
4、填空题 Ⅰ.在下图的装置中,属于原电池的是 。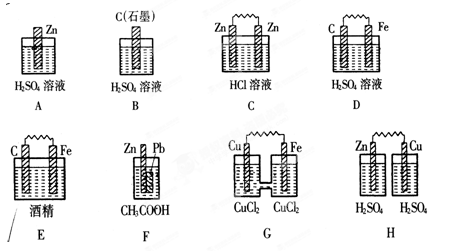
Ⅱ.(1)如图所示,烧杯中为CuCl2溶液,在图中画出必要的连线或装置,使连接后的装置为原电池。电极反应方程式:
铁板: ;碳棒: 。
(2)铜片、锌片连接后浸入稀硫酸中构成原电池,当导线上通过3.01×1022个电子时,锌片质量减少________g。铜片表面析出氢气_________L(标准状况)。
参考答案:Ⅰ.D、F、G Ⅱ.(1)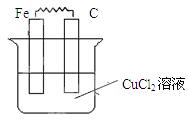 Fe-2e-=Fe2+ Cu2++2e-=Cu
Fe-2e-=Fe2+ Cu2++2e-=Cu
(2)1.625g 0.56L
本题解析:Ⅰ.原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,据此可知:
A、该装置只有一个电极材料,所以不能形成原电池;
B、该装置只有一个电极材料,且石墨和电解质溶液不能自发的进行氧化还原反应,所以不能形成原电池;
C、两电极材料相同,所以不能形成原电池,故错误;
D、该装置符合原电池的构成条件,所以能形成原电池,故正确;
E、酒精不是电解质,铁和酒精不能自发的进行氧化还原反应,所以不能形成原电池;
F、该装置符合原电池的构成条件,所以能形成原电池,故正确;
G、该装置符合原电池的构成条件,所以能形成原电池,故正确;
H、该装置两电极间不能构成闭合回路,所以不能形成原电池,所以答案选D、F、G
Ⅱ.(1)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。铁是活泼的金属,所以铁是负极,碳棒是正极,溶液中的铜离子再正极得到电子,发生还原反应,电极反应式分别是Fe-2e-=Fe2+、Cu2++2e-=Cu。
(2)铜片、锌片连接后浸入稀硫酸中构成原电池,其中锌是负极,铜是正极,电极反应式分别是Zn-2e-=Zn2+、2H++2e-=H2↑。3.01×1022个电子的物质的量是3.01×1022÷6.02×1023/mol=0.05mol,所以锌片质量减少0.025mol×65g/mol=1.625g,铜片表面析出氢气的体积(标准状况下)是0.025mol×22.4L/mol=0.56L。
考点:考查原电池构成条件的判断、电极反应式的书写以及有关计算等
点评:该题是高考中的常见考点,侧重对学生基础知识的巩固和训练。有利于培养学生的逻辑推理能力和规范答题能力。明确原电池的工作原理、构成条件是答题的关键,注意相关知识的积累和总结。
本题难度:一般
5、填空题 (16分)常见锌锰干电池因含有汞、酸或碱等,废弃后进入环境将造成严重危害。某化学兴趣小组拟采用如下处理方法回收废电池中的各种资源。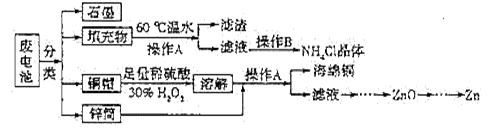
(1)填充物用60℃温水溶解,目的是 。
(2)操作A的名称为 。
(3)铜帽溶解时加入H2O2的目的是 (用化学方程式表示)。铜帽溶解完全后,可采用_____________方法除去溶液中过量的H2O2。
(4)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,其负极的电极反应式为 。
(5)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止。主要反应为2MnO(OH)+MnO2+2H2C2O4+3H2SO4=2MnSO4+4CO2↑+6H2O。
①当1 mol MnO2参加反应时,共有 mol电子发生转移。
②MnO(OH)与浓盐酸在加热条件下也可发生反应,试写出该反应的化学方程式: 。
(6)锌锰干电池所含的汞可用KMnO4溶液吸收。在不同pH下,KMnO4溶液对Hg的吸收率及主要产物如下图所示: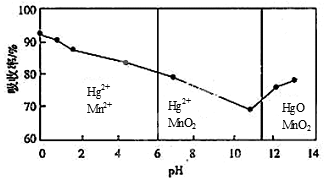
根据上图可知:
①pH对Hg吸收率的影响规律是随pH升高,汞的吸收率__ _.
②在强酸性环境下Hg的吸收率高的原因可能是KMnO4在酸性条件下 强.
参考答案:(16分) (1)加快溶解速率(1分);(2)过滤(1分)
(3)Cu+H2O2+H2SO4=CuSO4+2H2O(2分); 加热(2分);
(4)Zn+2OH--2e-=Zn(OH)2 (2分)
(5)①4(2分) ②2MnO(OH)+6HCl(浓) 2MnCl2+Cl2↑+4H2O (2分)
2MnCl2+Cl2↑+4H2O (2分)
(6)①先降低后增加(2分) ②氧化性(2分)
本题解析:(1)由于物质的溶解速率随温度的升高而增大。所以填充物用60℃温水溶解,目的是加快溶解速率;(2)分离难溶性固体与可溶性液体混合物的操作A的名称为过滤;(3)Cu不能溶于硫酸,在酸性条件下,加入H2O2的Cu就会被溶解变为Cu2+,反应的化学方程式是:Cu+H2O2+H2SO4=CuSO4+2H2O;H2O2不稳定,受热容易分解产生氧气和水,所以铜帽溶解完全后,可采用加热方法除去溶液中过量的H2O2。(4)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+ 2H2O=" 2MnOOH" +Zn(OH)2,其负极Zn发生氧化反应,电极反应式为Zn+2OH--2e-=Zn(OH)2;(5)①根据方程式2MnO(OH)+MnO2+2H2C2O4+3H2SO4=2MnSO4+4CO2↑+6H2O可知:当1 mol MnO2参加反应时,共有4mol的电子发生转移;②MnO(OH)与浓盐酸在加热条件下也可发生反应,则该反应的化学方程式是2MnO(OH)+6HCl(浓) 2MnCl2+Cl2↑+4H2O ;(6)①根据在不同pH下,KMnO4溶液对Hg的吸收率的示意图可知:pH对Hg吸收率的影响规律是随pH升高,汞的吸收率先降低后增加;在强酸性环境下Hg的吸收率高的原因可能是KMnO4在酸性条件下氧化性强的缘故。
2MnCl2+Cl2↑+4H2O ;(6)①根据在不同pH下,KMnO4溶液对Hg的吸收率的示意图可知:pH对Hg吸收率的影响规律是随pH升高,汞的吸收率先降低后增加;在强酸性环境下Hg的吸收率高的原因可能是KMnO4在酸性条件下氧化性强的缘故。
考点:考查反应条件的选择的原因分析、分离混合物的方法、原电池的电极反应式的书写、氧化还原反应化学方程式和离子方程式的书写、电子转移的计算、物质的吸收率与溶液pH的关系的知识。
本题难度:困难
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点讲解《氧化还原反.. | |