1、实验题 淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去):
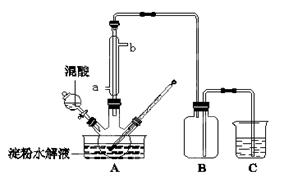
实验过程如下:
①将1∶1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30 min,然后逐渐将温度降至60℃左右;
②将一定量的淀粉水解液加入三颈烧瓶中;
③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO34的质量比为2:1.5)溶液;
④反应3h左右,冷却,减压过滤后再重结晶得草酸晶体。硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O?
C6H12O6?+8HNO3→6CO2+8NO↑+10H2O?
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
请回答下列问题:
(1)实验①加入98%硫酸少许的作用是:?。
(2)实验中若混酸滴加过快,将导致草酸产量下降,其原因是?。
(3)检验淀粉是否水解完全所用的试剂为?。
(4)草酸重结晶的减压过滤操作中,除烧杯、玻璃棒外,还必须使用属于硅酸盐材料的仪器有?。
(5)将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸。用KMnO4标准溶液滴定,该反应的离子方程式为:?
2MnO4- + 5H2C2O4 + 6H+ = 2Mn2+ + 10CO2↑+ 8H2O称取该样品0.12 g,加适量水完全溶解,然后用0.020 mol・L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),此时溶液颜色变化为?。滴定前后滴定管中的液面读数如图所示,则该草酸晶体样品中二水合草酸的质量分数为?。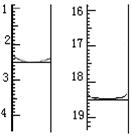
参考答案:(1)淀粉水解的速度(或起到催化剂的作用)
(2)温度过高、硝酸浓度过大,导致H2C2O4进一步被氧化
(3)碘水或KI-I2溶液
(4)布氏漏斗、吸滤瓶(安全瓶、抽气泵不作为主要仪器)
(5)无色突变为淡紫色且半分钟不褪色? 84.0%
本题解析:(1)淀粉水解需要浓硫酸作催化剂,即浓硫酸的作用是提高淀粉水解的速度(或起到催化剂的作用)。
(2)由于温度过高、硝酸浓度过大,会导致产物H2C2O4进一步被氧化,所以不能滴入的过快。
(3)由于碘能和淀粉发生显色反应,所以可以用碘水来检验淀粉是否完全水解。
(4)减压过滤时需要布氏漏斗、吸滤瓶。
(5)由于酸性高锰酸钾溶液是显紫红色的,所以当反应达到终点时,溶液颜色由无色突变为淡紫色且半分钟不褪色。根据滴定管的读数可知,消耗高锰酸钾溶液是18.50ml-2.50ml=16.00ml。根据方程式可知,草酸的物质的量是0.020 mol・L-1×0.016L×5/2=0.0008mol,则草酸晶体样品中二水合草酸的质量分数为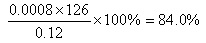
本题难度:一般
2、选择题 用下列实验装置进行相应实验,能达到实验目的的是(?)
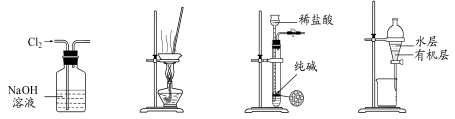
图1?图2?图3?图4
A.用图1 所示装置除去Cl2中含有的少量HCl
B.用图2 所示装置蒸发结晶提纯后的粗盐溶液,得NaCl晶体
C.用图3 所示装置制取少量纯净的CO2气体
D.用图4 所示装置分离用苯萃取碘水后已分层的有机层和水层
参考答案:B
本题解析:A不正确,因为氯气也能被氢氧化钠溶液吸收,应该用饱和食盐水;C不正确,氧气碳酸钠不是块状固体,极易溶于水,不能起到简易启普发生器的作用。苯的密度小于水的,因此有机层在上层,D不正确,答案选B。
点评:化学实验常用仪器的使用方法和化学实验基本操作是进行化学实验的基础,对化学实验的考查离不开化学实验的基本操作,所以该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。
本题难度:一般
3、选择题 下列各组物质中,气体X和气体Y在通常条件下同时通入盛有溶液Z的洗气瓶中(如图所示),一定没有沉淀生成的是(? )(已知常温下NaHCO3的溶解度小于Na2CO3、NaCl、NH4Cl、(NH4)2CO3和NH4HCO3的溶解度)
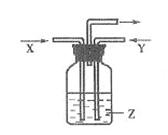
?
| X
| Y
| Z
|
A.
| NO2
| SO2
| BaCl2
|
B.
| NH3
| O2
| Al2(SO4)3
|
C.
| NH3
| CO2
| NaCl(饱和)
|
D.
| CO
| O2
| Ca(OH)2
参考答案:D
本题解析:NO2溶于水生成硝酸,硝酸氧化SO2生成硫酸,所以选项A中生成硫酸钡白色沉淀;氨气溶于水生成氨水,氨水和硫酸铝反应生成氢氧化铝白色沉淀;由于碳酸氢钠的溶解度小于Na2CO3、NaCl、NH4Cl、(NH4)2CO3和NH4HCO3的溶解度,所以选项C中有碳酸氢钠晶体析出;CO和氧气不点燃是不能反应生成CO2的,所以选项D中没有沉淀产生,答案选D。
本题难度:一般
4、选择题 [2012・淮安二模]下列有关实验原理或实验操作正确的是(?)
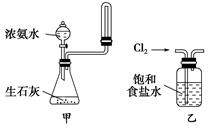
A.在蒸发皿中灼烧CuSO4・5H2O晶体以除去结晶水
B.用量筒量取20 mL 0.500 0 mol・L-1 H2SO4溶液于烧杯中,加水80 mL,配制成0.100 0 mol・L-1 H2SO4溶液
C.实验室用图甲所示的装置制取少量氨气
D.实验室用图乙所示的装置除去Cl2中的少量HCl
参考答案:D
本题解析:灼烧CuSO4・5H2O晶体除去结晶水应用坩埚,A项错;配制100 mL 0.100 0 mol・L-1的硫酸溶液应该用容量瓶,且液体混合后体积小于混合前两液体体积之和,B项错;收集气体的试管管口不能塞住,C项错误;实验室制氯气时,用饱和食盐水除去氯气中的氯化氢气体,D项正确。
新课标高三配套月考四化学试题(B卷)(带解析)
本题难度:一般
5、选择题 培养明矾晶体,为使晶体颗粒结得大一些,不应采取的方法是
A.用比室温约高10~20℃的水溶解明矾晶体得到饱和溶液
B.使明矾饱和溶液急速冷却
C.选用形状较为规则的小明矾晶体作晶核
D.结晶过程中,应将硬纸板盖住盛有饱和溶液的烧杯
参考答案:B
本题解析:该实验的成败关键是:1.所用试剂必须纯净,如含有杂质就很难获得完整的晶形。2.控制溶液的浓度,如果溶液过浓,析晶速率太快,不易形成晶形完整的晶体;3.如超过饱和溶液浓度不大,结晶速率太慢,小晶体慢慢长大。3.注意环境温度的变化,应使饱和溶液缓慢冷却。4.所用容器必须洁净,要加盖以防灰尘落入,所以选项B是错误的,答案选B。
点评:该题紧扣教材,基础性强,难度不大。试题贴近生活实际,有利于调动学生的学习兴趣,激发学生的学习积极性,提高学生的学习效率。
本题难度:一般
|