1��ѡ���� ���������У���ȷ����
A��0.1 mol?L��1 CH3COOH��Һ��ˮϡ��ʱ���������ӵ�Ũ�ȶ���С
B��NH4Cl��Һ�����Ե�ԭ��NH4+ + H2O  NH3��H2O + H+
NH3��H2O + H+
C��0.2 mol?L��1����������0.05 mol?L��1 Ba(OH)2��Һ��Ϻ���ҺpHΪ1
D��25��ʱpH=3�Ĵ�����Һ��pH=11������������Һ�������Ϻ�pH=7
2��ѡ���� �����й�����Ũ�ȹ�ϵ����������ȷ����? (����)��
A��25 ��ʱ��NaB��Һ��pH��8��c(Na��)��c(B��)��9.9��10��7mol��L��1
B��25 ��ʱ����0.1 mol��L��1NH4HSO4��Һ�еμ�NaOH��Һ�����ԣ�c(Na��)>c(NH4+)>c(SO42��)>c(OH��)��c(H��)
C��0.1 mol��L��1NaHCO3��Һ�У�c(OH��)��2c(CO32��)��c(H��)��c(H2CO3)
D��ͬ���£�pH��ͬʱ����Һ���ʵ���Ũ�ȣ�c(CH3COONa)>c(NaHCO3)>c(C6H5ONa)>c(Na2CO3)
3��ѡ���� ��100mL 1mol��L-1��Na2CO3��Һ������˵������ȷ����
A������Һϡ�ͣ�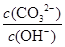 ����
����
B�����˺�0.l mol CH3COOH����Һ:c ( CH3 COOһ)��c( HCO3һ)
C��ͨ��0.1 mo1CO2���壬��Һ�д���:c ( Na+)��c( CO32һ)ʮc( HCO3һ)+c(H2CO3)
D�����˷�̪���ȣ���Һ��ɫ����
4��ѡ���� �������Һ����������֮������ֻ������˼����������ᵽ������Ȥ�����й��ڵ������Һ����������ȷ����
A��Na2CO3��NaHCO3��������Һ�У����������ͬ
B�������£�1mol/L��CH3COOH��Һ��1mol/L��NaOH��Һ�������ϣ����û��Һ�У�c(Na+) ��c(CH3COO-) ��c��H+����c(OH-)
C�����ʵ���Ũ����ͬ��NH4Cl��NH4HSO4������Һ�У�c(NH4+)ǰ��С�ں���
D�������£�ij��Һ����ˮ�������c(H+)=10-51mol��L-1�������Һ����������
5������� ��12�֣��ڳ����£�����������Һ����0.1mol/L NH4Cl?��0.1mol/L CH3COONH4?��0.1mol/L NH4HSO4?
�����Ҫ����д���пհף�
��1����Һ�ٳ�??�ԣ���ᡱ��������С�������ԭ���ǣ�
?�������ӷ���ʽ��ʾ��
��2��������������Һ�У�pH��С����?��c(NH4+)��С����??�z����ũ{
��3�������£������Һ�ڵ�pH=7����˵��CH3COO����ˮ��̶�________���������������������NH4+��ˮ��̶ȣ�CH3COO����NH4+Ũ�ȵĴ�С��ϵ�ǣ�
c(CH3COO��) ??c��NH4+)���������������������