|
高考化学知识点整理《常见的化学电源》高频试题预测(2019年最新版)(八)
2019-07-03 23:42:13
【 大 中 小】
|
1、选择题 RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池,RFC工作原理见图。下列有关说法正确的是
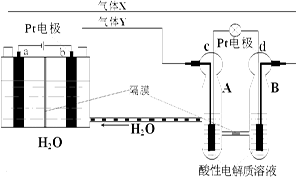
A.转移0.1mol电子时,a电极产生标准状况下O2 1.12L
B.b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH-
C.c电极上进行还原反应,B池中的H+可以通过隔膜进入A池
D.d电极上发生的电极反应是:O2+4H++4e-=2H2O
|
参考答案:C
本题解析:A.根据结构装置可知a是阴极,b是阳极,c是正极,d是负极。若转移0.1mol电子时,阴极a电极产生d的H2在标准状况下1.12L,错误;B.b电极是阳极,在阳极上发生氧化反应,电极反应是: 4OH--4e-=2H2O+O2↑,错误;C.c电极上通入的是O2,得到电子,进行还原反应产生OH-,根据同种电荷相互排斥,异种电荷相互吸引的原则,B池中的H+可以通过隔膜进入A池,正确;D.d电极是负极,在负极上发生氧化反应,该电极反应是:H2-2e-=2H+,错误。
考点:考查燃料电池、电解池的反应原理及应用的知识。
本题难度:困难
2、实验题 锂离子电池的广泛应用使回收利用锂资源成为重要课题:某研究性学习小组对废旧锂离子电池正极材料(LiMn2O4、碳粉等涂覆在铝箔上)进行资源回收研究,设计实验流程如下:

(1)第②步反应得到的沉淀X的化学式为?。
(2)第③步反应的离子方程式是?。
(3)第④步反应后,过滤Li2CO3所需的玻璃仪器有?。
若过滤时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因:
?、?。
(4)若废旧锂离子电池正极材料含LiMn2O4的质量为18.1 g,第③步反应中加入20.0mL 2.5mol・L-1的H2SO4溶液。正极材料中的锂经反应③和④完全转化为Li2CO3,至少有?g Na2CO3参加了反应。
参考答案:(1)Al(OH)3(2分)
(2)4 LiMn2O4+O2+4H+=4Li++8MnO2+2H2O?(2分)
(3) 漏斗玻璃棒烧杯(3分);?滤纸破损、滤液超过滤纸边缘等(2分)
(4)5.3(2分)
本题解析:正极材料包括LiMn2O4、碳粉、铝箔,其中的铝箔可溶合地碱液:①2Al+2NaOH+2H2O=2NaAlO2+3H2↑
过滤后,向滤液中通入过量的CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故沉淀X为Al(OH)3;滤渣为LiMn2O4、碳粉,向加稀硫酸并通入空气LiMn2O4溶解:4 LiMn2O4+O2+4H+=4Li++8MnO2+2H2O,过滤得到滤渣MnO2及碳粉;滤液加入碳酸钠:2Li++CO32-=Li2CO3↓,过滤可得到Li2CO3
过滤过程中所需要的玻璃仪器包括漏斗玻璃棒烧杯;若过滤时发现滤液中有少量浑浊,可能是由于滤纸破损、滤液超过滤纸边缘等原因造成
本题难度:一般
3、选择题 下图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是
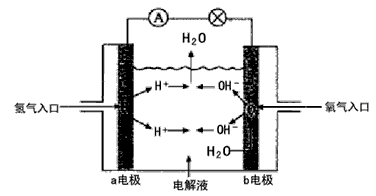
[? ]
A.a电极是负极
B.b电极的电极反应为: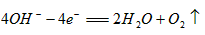
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
参考答案:B
本题解析:
本题难度:一般
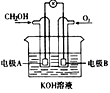
4、选择题 下图是一燃料电池化学原理示意图,该燃料电池总反应化学方程式为:
2CH3OH+3O2+4KOH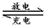 2K2CO3+6H2O以下判断不合理的是 2K2CO3+6H2O以下判断不合理的是
[? ]
A.电极A为电池负极
B.电极B表面上发生还原反应
C.溶液pH保持不变
D.燃料电池工作时不会出现火焰
参考答案:C
本题解析:
本题难度:一般
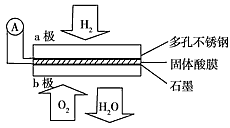
5、选择题 某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:
2H2+O2===2H2O,下列有关说法正确的是
[? ]
A. 电子通过外电路从b极流向a极
B. b极上的电极反应式为:O2+2H2O+4e-===4OH-
C. 每转移0.1 mol电子,消耗1.12 L的H2
D. H+由a极通过固体酸电解质传递到b极
参考答案:D
本题解析:
本题难度:一般
|