1��ѡ���� ��пƬ��ͭƬ�õ������Ӻ����ϡ������Һ�з���ԭ��ط�Ӧ������������ȷ���ǣ�������
A������������SO42-Ũ��������
B��������O2�ݳ�
C������ͨ��������ͭƬ����пƬ
D��ͭƬ����H2�ݳ�
�ο��𰸣�A��ԭ��طŵ�ʱ����Һ�����������ƶ�����������������SO42-Ũ��������A��ȷ��
B�������������ӵõ���������������B����
C��ԭ��طŵ�ʱ�����ӴӸ����ص�������������������ͨ��������пƬ����ͭƬ����C����
D��ͭƬ�������������������ӵõ���������������D��ȷ��
��ѡAD��
���������
�����Ѷȣ���
2��ѡ���� ����ͼ��ʾ�����м׳ص��ܷ�ӦʽΪ��2CH3OH��3O2��4KOH��2K2CO3��6H2O
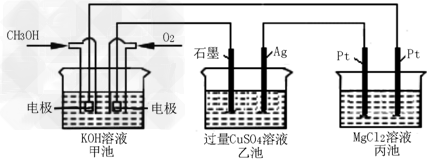
����˵����ȷ����
[? ]
A���׳��ǵ���ת��Ϊ��ѧ�ܵ�װ�ã��ҡ������ǻ�ѧ��ת�����ܵ�װ��
B���׳�ͨ��CH3OH�ĵ缫��ӦΪCH3OH��6e����2H2O��CO32����8H+
C����Ӧһ��ʱ������ҳ��м���һ����Cu(OH)2���壬��ʹCuSO4��Һ�ָ���ԭŨ��
D���׳�������280mL����״���£�O2����ʱ������������������1.45g����
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3��ѡ���� ��A��B��C��D�Ŀ����Ƭ����������ʵ�飺��A��B�õ���������ͬʱ����ϡ������Һ�У�AΪ��������C��D�õ���������ͬʱ����ϡ������Һ�У�������D�����ߡ�C����A��C������ͬʱ����ϡ������Һ�У�C�������������ݣ���B��D�õ���������ͬʱ����ϡ������Һ�У�D������������Ӧ���ݴˣ��ж����ֽ����Ļ��˳����
[? ]
A��A��B��C��D
B��A��C��D��B
C��C��A��B��D
D��B��D��C��A
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4��ѡ���� ��A��B��C��D���ֽ�������A��B�õ�����������������������Һ�У�B���ױ���ʴ����A��D�ֱ�Ͷ�뵽��Ũ�ȵ������У�D��A��Ӧ���ң���ͭ����B������Һ�������Ա仯����ͭ����C������Һ�У��н���C�������ݴ˿���֪���ǵĽ��������ǿ������˳��Ϊ(��? )
A��D��C��A��B? B��D��A��B��C? C��D��B��A��C? D��B��A��D��C
�ο��𰸣�B
���������A��B�γ�ԭ��أ�B���ױ���ʴ˵�����A>B��D��A�����ᷴӦ����˵�����D>A��ͭ�����û���B˵�����Cu<B��ͭ���û���C˵�����Cu>C�����Ͽ�֪���D>A>B>Cu>C��
������ԭ����и���ʧ���ӱ������������ܵ�������
�����Ѷȣ�һ��
5��ѡ���� ����˵����ȷ����
����25 mL��ʽ�ζ��ܿ���ȷ�ų�8.00 mL��ϡ���
�ڿ��ø����pH��ֽ�ⶨ��ˮ��pH��
��ʹ������ƿ������Һ������ʱ���ӣ�������Һ��Ũ��ƫ��
�ܼ�����������ʹ����ʯ��ˮ����ǵ���ɫ�������ɣ���ԭ��Һ�С����д���CO32-���ڣ�
����ij�¶��£�һ�����Ĵ���������������Һ��ֻ�ϣ�����Һ�ʼ���ʱ����Һ������Ũ�ȴ�С�Ĺ�ϵһ��Ϊ��c��Na������c��CH��COO������c��OH������c��H������
����ͼ�Ƿ�Ӧ���������������仯ʾ��ͼ������ܷ�����Ӧ���Ȼ�ѧ����ʽ�ɱ�ʾΪ��2 A��g��+ B(g) =" 2" C��g������H="Q" kJ��mol-1��Q��0 ����
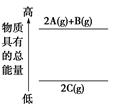
A���٢ۢ�
B���ڢܢ�
C���٢ۢ�
D���ۢݢ�
�ο��𰸣�A
����������ٵζ��ܾ���Ϊ0.01ml����ȷ������ˮ����Ư���ԣ��ʲ��ܲ����pH���۶��ݸ��ӣ����ƫС��Ũ��ƫ�ܲ�һ�������п���Ϊ̼���������������ȣ��ݸ��ݵ���غ㣬��ȷ���÷�ӦΪ���ȣ���Q<0��
�����Ѷȣ�һ��