1������� ��Դ���������Ϊ��Լ������ᾭ�÷�չ��ƿ����Խ��Խ��Ĺ��ҿ�ʼʵ�С�����ƻ���������̫������Դ��Ѱ�÷�չ���¶�����
��1��̫������ˮ���г�ʹ��һ�����������Ͻ������Ϊ���ռ���̫��������Ϳ�㣬д����̬��ԭ�ӵĺ�������Ų�ʽ_______________________��
��2������ϩ���������ھ������õĹ�����ܣ���̫���ܵ�ص�Ӧ���Ͼ��зdz�������ǰ;������ϩ
��C60���Ľṹ��ͼ��������̼ԭ�ӹ�����ӻ�����Ϊ_____________��1 mol C60�����ЦҼ�����ĿΪ
_____________��

��3����Ԫ�����ﱡĤ̫���ܵ�ز���Ϊ���Σ�����Ҫ�����黯�ء����ӡ���п��ͭ������Ĥ��صȡ�
�� ��һ�����ܣ�As________Se�����������������������
�� �����������ӵĿռ乹��Ϊ___________��
��4������̪ݼ������ڹ�̫���ܵ��������Ҫ���ã�һ�ֽ���þ̪ݼ�����Ľṹ����ͼ��������ͼ���ü�ͷ��ʾ����λ����
�ο��𰸣���1��1s22s22p63s23p63d84s2
��2��sp2��90NA
��3���٣����������� ��4��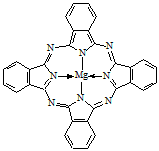
���������
�����Ѷȣ�����
2��ѡ���� ���и����Ӳ��в�����d�ܼ�����
[? ]
A.N��
B.M��
C.L��
D.K��
�ο��𰸣�CD
���������
�����Ѷȣ���
3������� X��Y��Z��QΪ�����ڷǽ���Ԫ�أ�R�dz�����Ԫ�أ�Xԭ�ӵĵ���ռ��2�����Ӳ���ԭ���гɶԵ�������δ�ɶԵ�������2����Y�Ļ�̬ԭ����7�ֲ�ͬ�˶�״̬�ĵ��ӣ�ZԪ���ڵؿ��к�����ࣻQ�ǵ縺������Ԫ�أ�R+����ֻ���������Ӳ�����ȫ�������ӣ�
��ش��������⣺������ʱ��X��Y��Z��Q��R������Ӧ��Ԫ�ط��ű�ʾ��
��1��R�Ļ�̬ԭ�ӵĵ����Ų�ʽΪ______��
��2��X��Y��Z����Ԫ�ص�һ�����ܴӴ�С˳��Ϊ______��
��3����֪Y2Q2���Ӵ�����ͼ��ʾ�����ֽṹ�����ģ�ͣ����߲�һ��������������
�ٸ÷���������Yԭ��֮��ļ��������ȷ����______
A����1���Ҽ�B.1���Ҽ���2���м�
C.1���Ҽ���1���м�D����2���Ҽ�
�ڸ÷�����Yԭ�ӵ��ӻ���ʽ��______
��4��R2+ˮ��Һ�д������������[R��H2O��4]2+���뻭��[R��H2O��4]2+���ӵĽṹʽ______
��5��X��YԪ�ؿ����γ�һ�ֳ�Ӳ�²��ϣ��侧�岿�ֽṹ��ͼ��ʾ���йظþ����˵����ȷ����______

A���þ������ڷ��Ӿ���
B���˾����Ӳ�ȱȽ��ʯ����
C������Ļ�ѧʽ��X3Y4
D�������ۻ�ʱ���ۼ����ƻ���û�п˷����»����������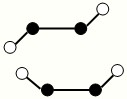
�ο��𰸣�X��Y��Z��QΪ�����ڷǽ���Ԫ�أ�R�dz�����Ԫ�أ�
Xԭ�ӵĵ���ռ��2�����Ӳ���ԭ���гɶԵ�������δ�ɶԵ�������2������Ϊ�ǽ�������XΪCԪ�أ�Y�Ļ�̬ԭ����7�ֲ�ͬ�˶�״̬�ĵ��ӣ���YΪNԪ�أ�
ZԪ���ڵؿ��к�����࣬��ZΪOԪ�أ�Q�ǵ縺������Ԫ�أ���QΪFԪ�أ�R+����ֻ���������Ӳ�����ȫ�������ӣ���RΪCuԪ�أ��ɷ�����֪��XΪCԪ�أ�YΪNԪ�أ�ZΪOԪ�أ�QΪFԪ�أ�RΪCuԪ�أ�
��1��RΪCuԪ�أ���̬ԭ�ӵĵ����Ų�ʽΪ1s22s22p63s23p63d104s1���ʴ�Ϊ��1s22s22p63s23p63d104s1��
��2��ͬ����Ԫ�ش�����Ԫ�صĵ�һ��������С����CԪ�ص���С������N��2p�������Ϊ�����״̬������ʧȥ���ӣ�
��һ�����ܴ���O�����Ե�һ�����ܴӴ�С��˳��Ϊ��N��O��C���ʴ�Ϊ��N��O��C��
��3��Y2Q2ΪN2F2������ͼ2�ֽṹ��Nԭ��֮���γ�N�TN˫������Nԭ��֮���γ�N�TN˫��������1���Ҽ���1���м�����ѡC��
���ӻ������=�Ҽ���+�¶Ե��Ӷ������÷�����Nԭ�ӵ��ӻ������=2+1=3������Nԭ���ӻ���ʽ��sp2�ӻ����ʴ�Ϊ��sp2�ӻ���
��4��[R��H2O��4]2+Ϊ[Cu��H2O��4]2+�����ӽṹʽΪ
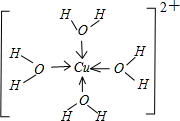
���ʴ�Ϊ��

��
��5��A��X��YԪ�ؿ����γ�һ�ֳ�Ӳ�²��ϣ��ɾ��岿�ֽṹ��֪���þ���Ϊԭ�Ӿ��壬��A����
B��C-N��������C-C�����̣�C-N�����ܴ����Ծ����Ӳ�ȱȽ��ʯ����B��ȷ��
C���ṹ��ÿ��Xԭ����Χ��4��Yԭ�ӣ�ÿ��Yԭ����Χ��3��Xԭ�ӣ����Ըþ��廯ѧʽΪX3Y4����ΪC3N4����C��ȷ��
D���þ���Ϊԭ�Ӿ��壬�����ۻ�ʱ���ۼ����ƻ���û�п˷����»������������D��ȷ��
�ʴ�Ϊ��BCD��
���������
�����Ѷȣ�һ��
4������� A��B��C��D��E���ֶ�����Ԫ�أ�ԭ��������������A��Eͬ���壬AԪ�ص�ԭ�Ӱ뾶��С��BԪ��ԭ�ӵ��������������ڲ��������2����CԪ��ԭ�ӵĵ��Ӳ���Ϊn������������Ϊ2n+1��A��B��C��Eÿ��Ԫ�ض�����DԪ��������ֻ��������ϵij���������ش��������⣺
��1��д�����и�Ԫ�ص����ƣ�A______?D______
��2����������Ԫ���У���һ��������С��Ԫ����______����̬ԭ��δ�ɶԵ���������ԭ�Ӻ�������Ų�ʽΪ______��
��3����֪��BA3DA��g��+A2D��g��=BD2��g��+3A2��g����H1=+49.0kJ/mol��BA3DA��g��+1/2D2��g��=BD2��g��+2A2��g����H2=-192.9kJ/mol����д������̬BA3DA��ȫȼ��������̬A2D���Ȼ�ѧ����ʽ�����Ƴ���Ԫ�ط�����д����______
��4���Կ��淴Ӧ3A2��g��+C2��g��?2CA3��g������Ӧ�ﵽƽ��λ��ʱ���ϸı����������ı�A2��C2��CA3����������ͼ��ʾ��Ӧ�����뷴Ӧ���̵Ĺ�ϵ�����б�ʾƽ��������CA3�ĺ�����ߵ�һ��ʱ����______����һ���¶��£�����4amol?A2��2a?mol?C2����lL���ܱ������У���ַ�Ӧ����C2��ת����Ϊ50%����÷�Ӧ��ƽ�ⳣ��Ϊ______������ʱ�����������Ͷ��a?mol?A2��a?mol?C2��2a?mol?CA3���ж�ƽ���ƶ�����______�����������桱���ƶ�������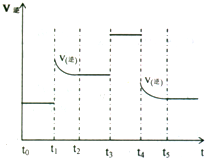
�ο��𰸣�Aԭ�Ӱ뾶��С����AΪHԪ�أ�BԪ��ԭ�ӵ��������������ڲ��������2������BΪCԪ�أ�CԪ��ԭ�ӵĵ��Ӳ���Ϊn������������Ϊ2n+1����nΪ2ʱ��CΪNԪ�أ���nΪ3ʱ��CΪClԪ�أ���������C����ΪCl������E�Ͳ��Ƕ�����Ԫ�أ�����CΪNԪ�أ�A��Eͬ���壬����EΪNaԪ�أ�A��B��C��Eÿ��Ԫ�ض�����DԪ��������ֻ��������ϵij����������DΪOԪ�أ�
��1���������ƶϿ�֪AΪHԪ�أ�DΪOԪ�أ���Ҫ��дԪ������Ϊ���� �����ʴ�Ϊ����? ����
��2�����ݵ�һ�����ܱ仯���ɣ����ڱ��У�ͬ���ڴ����ң�������������ͬ������ϵ��£���һ��������С������������Ԫ�����Ƶĵ�һ��������С��
H��C��N��O��Na������Ԫ�ص�δ�ɶԵ�������Ϊ��1��2��3��2��1��NԪ�ص�δ�ɶԵ�������࣬�����Ų�ʽΪ��1s22s22p3���ʴ�Ϊ��Na? 1s22s22p3��
��3������ĸ���ɾ���Ԫ�صã���CH3OH��g��+H2O��g��=CO2��g��+3H2��g������H=+49.0kJ?mol-1
��CH3OH��g��+12O2��g��=CO2��g��+2H2��g������H=-192.9kJ?mol-1
���ݸ�˹���ɽ��ڡ�3-�١�2�ɵã�CH3OH��g��+32 O2��g��=CO2��g��+2H2O��l��
��H=-192.9kJ/mol��3-49kJ/mol��2=-676.7kJ/mol��
�ʴ�Ϊ��CH3OH��g��+32 O2��g��=CO2��g��+2H2O��l����H=-676.7kJ/mol��
��4����ͼ��ɿ������ı�����ƽ��һֱ���淴Ӧ�����ƶ�����t0-t1 NH3������ߣ�
? ?3H2+N2=2NH3
��ʼŨ�ȣ�mol/L��? 4 a? 2a? 0?
ת��Ũ�ȣ�mol/L��?3a? a? 2a
ƽ��Ũ�ȣ�mol/L��? a? a? 2a
K=(2a)2a��a3=4a2������ʱ�����������Ͷ��a?mol?A2��a?mol?C2��2a?mol?CA3ʱ��
�൱�ڼ�ѹ��ƽ����������ٷ��������ƶ����ʴ�Ϊ��t0-t1 4a2����
���������
�����Ѷȣ�һ��
5��ѡ���� ����˵����ȷ����
[? ]
��ԭ���д���n=4״̬�ĵ���ԾǨ��n=3��״̬ʱ��Ҫ�ų�����
��n=4���ܲ�������ܼ�4s��4p�� 4d��4f��4g
��3pz��ʾ��3��pz���
����ԭ���У������ܳ����˶�״̬��ȫ��ͬ����������
��2s�����������ֿռ�ȡ��
A���٢�
B���ڢ�
C���٢ڢ�
D���ۢܢ�
�ο��𰸣�A
���������
�����Ѷȣ���