1、选择题 下列溶液中各微粒的浓度关系正确的是( )
A.0.1?mol?L-1Na2S溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S)
B.0.l?mol?L-1pH=9的NaNO2溶液中:c(Na+)>c(NO2-)>c(OH-)>c(H+)
C.等pH的氨水、NaOH溶液、Ba(OH)2溶液中:c(NH4+)=c(Na+)=c(Ba2+)
D.向NH4HCO3溶液中滴加NaOH溶液至pH=7:c(NH4+)+c(Na+)=c(HCO3-)+c(CO32-)
2、填空题 黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。
(1)将0.050 mol SO2(g)和0.030 mol O2(g)放入容积为1 L的密闭容器中,反应2SO2(g)+O2(g)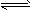 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高
SO2平衡转化率的有________(填字母)
(A)升高温度 (B)降低温度 (C)增大压强 (D)减小压强 (E)加入催化剂 (G)移出氧气
(3)SO2尾气用饱和Na2SO3溶液吸收可得到重要的化工原料,反应的化学方程式为_________________________________。
(4)将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需保持溶液足够酸性,其原因是_______________________。
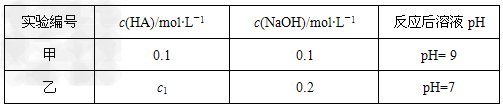
3、选择题 常温下,将某一元酸HA和NaOH溶液等体积混合,实验信息如下:下列判断不正确的是
[? ]
A.?c1一定大于0.2?mol・L-1
B.?HA的电离方程式是HA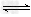 H+?+?A-
H+?+?A-
C.?甲反应后溶液中:c(Na+)?>?c(OH-)?>?c(A-)?>?c(H+)
D.?乙反应后溶液中:c(Na+)?<?c(HA)?+?c(A-)
4、选择题 在蒸发皿中用酒精灯加热并灼烧下列物质的溶液,可以得到该物质固体的是( )
A.氯化铝
B.碳酸氢钠
C.硫酸镁
D.高锰酸钾
5、选择题 下列有关电解质溶液中微粒的物质的量浓度关系不正确的是
[? ]
A.在0.1 mol.L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-)
B.在0.1 mol.L-1Na2CO3溶液中:c(OH -)-c(H+)=c(HCO3-)+2c(H2CO3)
C.向0.2 mol.L-1NaHCO3溶液中加入等体积0.1 mol.L-1NaOH溶液:c(CO32-)>c(HCO3-)> c(OH-)>c(H+)
D.常温下,pH =7的CH3 COONa和CH3 COOH的混合溶液:c(Na+)=c(CH3COO -)>c(H+) =c(OH -)