|
高中化学必备知识点《影响化学反应速率的因素》高频试题巩固(2019年最新版)(八)
2019-07-03 23:58:22
【 大 中 小】
|
1、选择题 四氯化硅还原法是当前制备较高纯度硅的一种方法,有关反应的化学方程式为:
SiCl4(g)+2H2(g) ="===Si" (s)+4HCl(g)。下列说法合理的是 ( )
A.光导纤维的主要成分是硅单质
B.减小压强有利于加快化学反应速率
C.高温下,氢气的还原性强于硅
D.混入少量空气对上述反应无影响
|
参考答案:C
本题解析:略
本题难度:一般
2、填空题 (5分)某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)(2分)硫酸铜溶液可以加快氢气生成速率的原因 。
(2)(1分)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是 。
(3)(2分)要加快上述实验中气体产生的速率,还可采取的措施有(答两种): ; 。
参考答案:(1)CuSO4与Zn反应生成的Cu附着在Zn表面形成铜锌原电池加快了化学反应速率;
(2)Ag2SO4;
(3)适当增加硫酸的浓度;增加锌粒的表面积;升高温度等(答两种即可)。
本题解析:(1)硫酸铜溶液可以加快氢气生成速率的原因是CuSO4与Zn反应生成的Cu附着在Zn表面形成铜锌原电池加快了化学反应速率。
(2)Ag2SO4与Zn反应生成的Ag附着在Zn表面形成银锌原电池加快了化学反应速率,所以与上述实验中CuSO4溶液起相似作用的是Ag2SO4;
(3)根据影响化学反应速率的因素可知,要加快上述实验中气体产生的速率,还可采取的措施有:适当增加硫酸的浓度;增加锌粒的表面积;升高温度等。
考点:理解外界条件(浓度、温度、压强、催化剂等)对反应速率的影响,认识并能用相关理论解释其一般规律。
点评:本题考查了影响化学反应速率的因素,特别是原电池对化学反应速率的影响。
本题难度:一般
3、选择题 用3g块状大理石与30mL3mol/L盐酸反应制取CO2气体,若要增大反应速率且不影响CO2气体的量,可以采用的措施是
[? ]
①再加入30mL3mol/L盐酸 ②改用30mL6mol/L 盐酸 ③改用3g粉末状大理石 ④适当升高温度
A.①④
B.②③④
C.③④
D.①③④
参考答案:B
本题解析:
本题难度:一般
4、选择题 C+CO2 2CO; △H1>0,反应速率ν1? N2+3H2 2CO; △H1>0,反应速率ν1? N2+3H2 2NH3;?△H2<0,反应速率ν2。如升温, 2NH3;?△H2<0,反应速率ν2。如升温,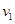 和 和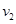 的变化是 的变化是
A.同时增大? B.同时减少?C,ν1增大,ν2减少? D.ν1减少,ν2增大
参考答案:A
本题解析:升高温度,化学反应速率都加快。这与反应是否是可逆反应无关,也跟正反应是放热反应还是吸热反应无关。所以正确选项为:A。
本题难度:一般
5、选择题 下列措施是为了降低化学反应速率的是( )
A.用铁粉代替铁钉与稀硫酸反应制取氢气
B.食品放在冰箱中贮藏
C.在试管中进行铝和盐酸反应时,稍微加热
D.合成氨工业中使用催化剂
参考答案:A、用铁粉代替铁钉与稀硫酸反应制取氢气时,由于反应物铁的表面积增大,所以反应速率加快,故A错误;
B、食品放在冰箱中贮藏时,由于温度降低而导致食物氧化变质的反应速率减慢,故B正确;
C、铝和盐酸反应时,稍微加热,能使化学反应速率加快,故C错误;
D、合成氨工业中使用催化剂,可以使反应速率加快,故D错误.
故选B.
本题解析:
本题难度:一般
|