| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《盐类水解的原理》高频考点巩固(2019年模拟版)(四)
参考答案:AD 本题解析:A、碳酸钠溶液中,根据质子守恒,则c(OH-)=c(H+)+c(HCO3-)+ 2c(H2CO3),所以有c(OH-)-c(H+)=c(HCO3-)+ 2c(H2CO3)成立,正确;B、浓度相同的产生和醋酸钠的混合液的pH<7,溶液为酸性,说明醋酸的电离程度大于醋酸根离子的水解程度,则c(CH3COO-)>c (Na+) >c(CH3COOH)>c(H+)>c(OH-),错误;C、浓度均为0.1 mol・L-1的NaClO、NaHCO3混合溶液中,Cl元素与C元素的浓度相等,所以c(HClO)+c(ClO-)=c(HCO3-)+ c(H2CO3)+ c(CO32-),错误;D、向0.1 mol/L NH4HSO4溶液中滴加NaOH溶液至中性,则c (OH-)=c(H+),根据电荷守恒,则2c(SO42-)+ c (OH-)=c(Na+)+c(NH4+)+c(H+),若溶液呈中性,则氢氧化钠的物质的量大于硫酸氢铵的物质的量,所以c(Na+)>c(SO42-)>c(NH4+)>c (OH-)=c(H+),正确,答案选AD。 本题难度:一般 4、选择题 25 ℃时,下列有关溶液中微粒的物质的量浓度关系正确的是 |
参考答案:BD
本题解析:根据电荷守恒可以判断A错误;根据电荷守恒和物料守恒可知B正确;pH=9.4说明水解大于电离,所以c(HCN) 的浓度大于c(CN-)故C错误;0.1 mol・L-1 CH3COONa 溶液与0.05 mol・L-1盐酸等体积混合后溶液中有CH3COOH为0.025mol・L-1、CH3COONa为0.025mol・L-1所以有c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)故D正确。
考点:溶液中微粒的浓度的大小比较
本题难度:困难
5、选择题 常温下,向10mL b mol・L-1的CH3COOH溶液中滴加等体积的0.0l mol・L-1的NaOH溶液,充分反应后溶液中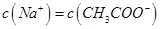 ,下列说法不正确的是
,下列说法不正确的是
A.b>0.0l
B.混合后溶液呈中性
C.CH3COOH的电离常数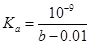 mol・L-1
mol・L-1
D.向CH3COOH溶液中滴加NaOH溶液的过程中,水的电离程度逐渐减小
参考答案:D
本题解析:因为CH3COOH为弱酸,NaOH为强碱,反应生成CH3COONa,根据电荷守恒可得c(Na+)+c(H+)=c(CH3COO?)+c(OH?),因为c(Na+)=c(CH3COO?),可得c(H+)=c(OH?),则混合后溶液呈中性,因为CH3COONa水解呈碱性,所以CH3COOH应过量,使溶液呈中性,所以b>0.0l,故A项、B项正确;反应后溶液呈中性,c(H+)=10-7mol?L?1,c(CH3COO?)= c(Na+)=1/2×0.01mol?L?1=0.005mol?L?1,c(CH3COOH)=1/2×(b―0.01)mol?L?1,所以CH3COOH的电离常数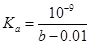 mol・L-1,故C正确;向CH3COOH溶液中滴加NaOH溶液的过程中,水的电离程度先增大,CH3COOH完全反应后,再滴加NaOH溶液,水的电离程度减小,故D项错误。
mol・L-1,故C正确;向CH3COOH溶液中滴加NaOH溶液的过程中,水的电离程度先增大,CH3COOH完全反应后,再滴加NaOH溶液,水的电离程度减小,故D项错误。
考点:本题考查弱电解质的电离平衡、盐类的水解、电离常数的计算。
本题难度:困难
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点归纳《原电池原理.. | |