1、选择题 下列相关反应的离子方程式书写正确的是(?)
A.氢氧化铁溶于氢碘酸:Fe(OH)3 +3H+ =Fe3++3H2O
B.NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3―+Ba2++2OH― = BaCO3? +2H2O+CO32―
C.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
D.向含有0.4 mol FeBr2的溶液中通入0.1 mol Cl2反应:2Fe2++Cl2=2Fe3+ +2Cl-
参考答案:D
本题解析:A、Fe3+与I-不能共存,错误;B、反应为HCO3―+Ba2++OH― = BaCO3? +H2O,错误;C、反应为Al3++NH4++2SO42-+2Ba2++4OH-=Al(OH)3↓+2BaSO4↓+NH3・H2O,错误。 D、Fe2+的还原性大于Br-,正确。
本题难度:一般
2、选择题 能用H++OH-=H2O表示的化学方程式是( )
A.氢氧化钠溶液与醋酸反应
B.氢氧化铁与硫酸反应
C.氢氧化钡与硫酸反应
D.硫酸氢钠与氢氧化钠溶液反应
参考答案:A.醋酸为弱电解质,应写成化学式,不能用H++OH-=H2O表示,故A错误;
B.氢氧化铁难溶于水,应写成化学式,不能用H++OH-=H2O表示,故B错误;
C.氢氧化钡与硫酸反应生成硫酸钡沉淀和水,不仅仅发生H++OH-=H2O,故C错误;
D.硫酸氢钠与氢氧化钠溶液反应的离子方程式为H++OH-=H2O,故D正确.
故选D.
本题解析:
本题难度:简单
3、选择题 下列各组中的反应(反应在溶液中进行),可用同一离子方程式表示的是?(?)
A.NaOH+HCl;KOH+CH3COOH
B.NaOH+H2SO4;Ba(OH)2+H2SO4
C.BaCl2+H2SO4;Ba(OH)2+Na2SO4
D.CaCO3+H2SO4;Na2CO3+HCl
参考答案:C
本题解析:A项中CH3COOH应写化学式;B项中NaOH+H2SO4为H++OH-=H2O,Ba(OH)2+H2SO4为Ba2++2OH-+2H++ SO42-=BaSO4↓+2H2O;C项只是Ba2++SO42-=BaSO4↓;D项中CaCO3应写化学式,产物中CaSO4也写化学式。
本题难度:简单
4、填空题 (12分)
在盛有AgNO3、HCl、Na2CO3、CaCl2、NaCl五种无色溶液的试剂瓶上,分别贴有①~⑤的编号。将它们两两混合,产生的现象如表所列(其中“↑”表示产生气体,“↓”表示生成沉淀,“―”表示无现象):
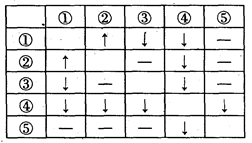
(1)写出③、④、⑤三种物质的化学式为:
③______________,④_____________,⑤_______________。
(2)写出下列反 应的离子方程式:①+②__________________________。
应的离子方程式:①+②__________________________。
参考答案:(1)③CaCl2?④AgNO3?⑤NaCl
(2)2H++CO32-=CO2↑+H2O
本题解析:略
本题难度:一般
5、选择题 下列方程式正确的是( )
A.热化学方程式C2H2(g)+
O2(g)=2CO2(g)+H2O(g)△H=-1256kJ/mol,表示乙炔的燃烧热为1256kJ/mol
B.高锰酸钾酸性溶液与草酸溶液反应:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
C.在稀氨水中通入少量CO2:2NH3?H2O+CO2=2NHH4++CO32-+H2O
D.用银氨溶液检验乙醛中的醛基:CH3CHO+2[Ag(NH3)2]++2OH-CH3COO-+NH4++3NH3+2Ag↓+H2O
参考答案:A、水的稳定状态时液态而不是气态,从气态水到液态水要放热,所以乙炔的燃烧热大于1256kJ/mol,故A错误;
B、草酸属于弱酸,弱酸在离子方程式中不能拆成离子的形式,应保留分子式不变,故B错误;
C、在稀氨水中通入少量CO2,碱性溶液和酸性气体反应得到盐,方程式为:2NH3?H2O+CO2=2NHH4++CO32-+H2O,故C正确;
D、银氨溶液具有弱氧化性,醛具有还原性,可以用银氨溶液检验物质中的醛基,现象是析出银镜,方程式为:CH3CHO+2[Ag(NH3)2]++2OH-△
本题解析:
本题难度:一般