1、选择题 N2+3H2 2NH3反应达到平衡时的说法不正确的是( )。
2NH3反应达到平衡时的说法不正确的是( )。
A.平衡体系中氮气、氢气、氨的物质的量保持不变
B.平衡体系中氮气、氢气、氨的浓度保持不变
C.单位时间内生成的氨和分解的氨物质的量相同
D.单位时间内消耗的氮气和氢气与生成的氨气物质的量相同
参考答案:D
本题解析:达到平衡时,各组分的物质的量、浓度都会保持不变。无论是平衡状态时还是非平衡状态时,单位时间内消耗N2、H2的物质的量跟生成NH3的物质的量都不可能相等。
本题难度:简单
2、选择题 在一定条件下,在容积为2L的密闭容器中,将2 mol 气体M和3 mol N气体混合,发生如下反应:2M(g) + 3N(g)  ?x Q(g) +3R(g),该反应达平衡时,生成2.4mol R,并测得Q的浓度为0.4 mol/L,下列有关叙述正确的是
?x Q(g) +3R(g),该反应达平衡时,生成2.4mol R,并测得Q的浓度为0.4 mol/L,下列有关叙述正确的是
A.x值为2
B.混合气体的密度增大
C.平衡时N的浓度为0.2 mol/L
D.N的转化率为80%
参考答案:D
本题解析:采用“三段式”计算
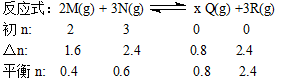
从以上数据可看出:x=1,平衡时N的浓度为0.3 mol/L,N的转化率为80%
由于气体的体积及质量均不变,故密度也是定值
答案为D
本题难度:一般
3、填空题 (14分)如图的甲、乙两容器,甲体积可变压强不变,乙保持体积不变。向两容器中分别充入1 mol A、3 mol B,此时两容器体积均为500 mL,温度为T℃。保持温度不变,发生反应A(g)+3B(g) 2C(g)+D(s);△H<0。
2C(g)+D(s);△H<0。
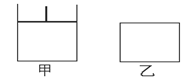
 (1)下列选项中,能表明甲和乙容器中反应一定达到平衡状态的是________。
(1)下列选项中,能表明甲和乙容器中反应一定达到平衡状态的是________。
A.混合气体的总质量不随时间改变? B.2 v正(C)=3 v逆(B)
C.A、B转化率相等? D. 物质D的质量不随时间改变
(2)2 min后甲容器中的化学反应达到平衡, 测得C
测得C 的浓度为2 mol/L,此时容器的体积为________mL,B的转化率α甲(B)为________。
的浓度为2 mol/L,此时容器的体积为________mL,B的转化率α甲(B)为________。
(3)乙容器中反应 达到平衡所需要的时间______2 min(填“>、<或=”),B的转化率α
达到平衡所需要的时间______2 min(填“>、<或=”),B的转化率α 乙(B) ______α甲(B) (填“>、<或=”)。
乙(B) ______α甲(B) (填“>、<或=”)。
(4)若其它条件不变,甲中如果从逆反应方向开始反应建立平衡,要求平衡时C的物质的量与(2)中平衡时C的物质的量相等,则需要加入C的物质的量n(C)=________mol,加入D的物质的量n (D)应该满足的条件为________________________。
参考答案:(14分)
(1)A D
(2)400,40%
(3)>、<
(4)2,n (D)>0.6 mol
本题解析:略
本题难度:一般
4、简答题 (14分)研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:①Fe2O3(s) + 3C(石墨) =" 2Fe(s)" + 3CO(g)?△H 1 = +489.0 kJ・mol-1
?②C(石墨) +CO2(g) = 2CO(g)?△H 2 = +172.5 kJ・mol-1
则CO还原Fe2O3(s)的热化学方程式为?。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g) CH3OH(g) +H2O(g)?△H
CH3OH(g) +H2O(g)?△H
①该反应的平衡常数表达式为K=???。
②取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中,发生上述反应反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的ΔH?0 (填“>”、“<”或“=”)。

③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ?KⅡ(填“>”、“<”或“=”)。
(3)以CO2为原料还可以合成多种物质。
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成,其反应方程式为?。
当氨碳比 =3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为:?。
=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为:?。
②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,该电极反应的方程式为?。
参考答案:(1)Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g)?△H?= ―28.5 kJ・mol-1
(2)①? ?;②< ; ③>
?;②< ; ③>
(3)(2)2NH3+CO2 CO(NH2)2+H2O? 40 %?②CO2+8e―+8H+=CH4+2H2O
CO(NH2)2+H2O? 40 %?②CO2+8e―+8H+=CH4+2H2O
本题解析:(1) ①-②×3,整理可得Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g)?△H?= ―28.5 kJ/mol。(2)①化学平衡常数是可逆反应达到平衡状态时各种生成物浓度的幂指数的乘积与各种反应物浓度的幂指数的乘积的比。对该反应来说,K= 。②由甲醇的体积分数φ(CH3OH)与反应温度T的关系图示可知:当反应达到平衡后,升高温度,甲醇的体积分数减小,说明升高温度,化学平衡逆向移动。根据偏高移动原理:升高温度梦幻西游平衡向吸热反应方向移动。逆反应方向为吸热反应,所以正反应为放热反应。所以ΔH<0。 ③曲线Ⅱ比I先达到平衡。说明温度温度曲线Ⅱ>I。由于温度高,CH3OH含量低,说明化学平衡常数KⅠ>KⅡ。(3)①根据质量守恒定律,由CO2和NH3在一定条件下合成尿素[CO(NH2)2]的反应方程式为2NH3+CO2
。②由甲醇的体积分数φ(CH3OH)与反应温度T的关系图示可知:当反应达到平衡后,升高温度,甲醇的体积分数减小,说明升高温度,化学平衡逆向移动。根据偏高移动原理:升高温度梦幻西游平衡向吸热反应方向移动。逆反应方向为吸热反应,所以正反应为放热反应。所以ΔH<0。 ③曲线Ⅱ比I先达到平衡。说明温度温度曲线Ⅱ>I。由于温度高,CH3OH含量低,说明化学平衡常数KⅠ>KⅡ。(3)①根据质量守恒定律,由CO2和NH3在一定条件下合成尿素[CO(NH2)2]的反应方程式为2NH3+CO2 CO(NH2)2+H2O。
CO(NH2)2+H2O。 =3,假设n(CO2)=amol,则n(NH3)=3amol。由于达平衡时CO2的转化率为60%,所以反应消耗的n(CO2)=0.6amol.,根据方程式中二者的物质的量的关系可知反应的NH3的物质的量n(NH3)=1.2amol.所以氨气的转化率为(1.2amol.÷3amol)×100%=40%.②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,则根据题意可得:该电极反应的方程式为CO2+8e―+8H+=CH4+2H2O。
=3,假设n(CO2)=amol,则n(NH3)=3amol。由于达平衡时CO2的转化率为60%,所以反应消耗的n(CO2)=0.6amol.,根据方程式中二者的物质的量的关系可知反应的NH3的物质的量n(NH3)=1.2amol.所以氨气的转化率为(1.2amol.÷3amol)×100%=40%.②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,则根据题意可得:该电极反应的方程式为CO2+8e―+8H+=CH4+2H2O。
本题难度:一般
5、选择题 在一定温度下的密闭容器中,不能表明A(s)+2B(g) C(g)+D(g)已达平衡的是?
C(g)+D(g)已达平衡的是?
A.A的质量不再发生改变
B.气体的总物质的量不再发生改变
C.C的分子数不再发生改变
D.D的物质的量浓度不再发生改变
参考答案:B
本题解析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,所以选项ACD都可以说明。反应前后气体的体积不变,因此气体的总物质的量始终是不变的,B不能说明,答案选B。
点评:该题是中等难度的试题,该题也是高考中的常见题型和考点。试题基础性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确平衡状态的特点,如何结合具体的可逆反应灵活运用即可。
本题难度:简单