1、简答题 (10分)1965年合成了催化剂A,实现了温和条件下的烯烃加氢。
5-1 A是紫红色晶体,分子量925.23,抗磁性。它通过RhCl3・3H2O和过量三苯膦(PPh3)的乙醇溶液回流制得。画出A的立体结构。
5-2 A可能的催化机理如下图所示(图中16e表示中心原子周围总共有16个电子):
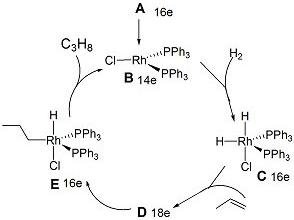
画出D的结构式。
5-3 确定图中所有配合物的中心原子的氧化态。
5-4 确定A、C、D和E的中心离子的杂化轨道类型。
5-5 用配合物的价键理论推测C和E显顺磁性还是抗磁性,说明理由。
参考答案:(10分)
5-1 A:
5-2 D: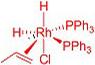
5-2 A? +1? B? +1? C? +3? D? +3? E? +3
5-4 A? d2sp3? C? dsp3? D? d2sp3? E? dsp3
5-5 顺磁性?理由可由下图表达:
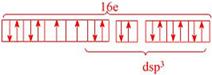
本题解析:略
本题难度:一般
2、选择题 能够证明电子在原子核外是分层排布的事实是( )
A.电负性
B.电离能
C.第一电离能
D.原子半径
参考答案:B
本题解析:能够证明电子在原子核外是分层排布的事实是电离能,电负性为吸引电子的能力。
本题难度:简单
3、选择题 2H、13C、15N、18O、34S等常用作环境分析指示物,下列对它们的说法正确的是
A.34S原子核内的中子数为16?B.16O与18O互称同位素
C.13C和15N原子核内的质子数相差2? D.2H的核外电子数比1H多一个
参考答案:B
本题解析:在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数。又因为质子数和中子数之和是质量数,所以选项A中中子数是34-16=18,A不正确;质子数相同而中子数不同的同一种元素的不同核素互为同位素,所以B正确。C不正确,二者的质子数相差1,C不正确;2H的核外电子数和1H的核外电子数相同,都是1,答案选B。
点评:该题是基础性试题的考查,侧重对学生基础知识的巩固和训练。该题的关键是明确同位素、核素的含义以及原子组成的表示方法,并能灵活运用即可。
本题难度:简单
4、填空题 (10分)按要求回答下列问题:
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是?
(2)用电子式表示下列化合物的形成过程
H2S?;MgF2?
(3)写出2,2,4―三甲基-3-乙基庚烷的结构简式:?
(4)写出(CH3)2CHCH(CH3)(CH2)3CH3 的名称:?
参考答案:(10分)、(1)略? (2)略? (3) (CH3)3CCH(CH2CH3)CH(CH3)CH2CH2CH3
(4) 2,3―二甲基庚烷(各2分)
本题解析:略
本题难度:简单
5、选择题 下列有关结构和性质的说法中不正确的是 ( )
A.元素周期表中从ⅢB族到ⅡB族十个纵行的元素都是金属元素
B.碱性:NaOH > NH3・H2O ,所以元素的金属性:Na > N
C.同周期第ⅡA族与第ⅢA族的元素原子序数之差不一定为1
D.第ⅦA族元素从上到下,其氢化物的稳定性逐渐减弱
参考答案:B
本题解析:A、正确;B、比较金属性强弱的依据是:最高价氧化物对应水化物的碱性强弱。而NH3・H2O不是氮元素的最高价氧化物对应水化物,故B错误;C、原子序数只差可能为1、11、25;D、从上到下,非金属性逐渐减弱,其氢化物的稳定性减弱。
本题难度:一般