1、选择题 甲、乙、丙、丁、戊五种溶液的溶质分别是HCl、CH3COOH、NaOH、NH3・H2O、Na2CO3中的一种。常温下如下实验:
①将0.1L?pH=9的甲溶液分别与a?L?0.001mol/L的乙溶液、b?L0.001lmol/L的丁溶液充分反应后溶液呈中性时,a>b;
②浓度均为0.1?mol/L的丙和丁溶液等体积混合后,溶液呈酸性;?
③0.1mol/L的甲溶液pH小于0.1mol/L?的戊溶液pH。
下列判断正确的是
[? ]
A.甲的溶质是NH3・H2O?
B.丙的溶质NaOH ?
C.乙的溶质是CH3COOH?
D.戊的溶质是HCl
参考答案:C
本题解析:
本题难度:一般
2、填空题 A、B、C、D、E五种溶液分别是NaOH、NH3?H2O、CH3COOH、HCl、NH4HSO4中一种.常温下进行下列实验:
①将1LpH=3的A溶液分别与0.001mol?L-1xLB溶液、0.001mol?L-1yLD溶液充分反应后溶液呈中性,x、y大小关系为:y<x;
②浓度均为0.1mol?L-1A和E溶液,pH:A<E;
③浓度均为0.1mol?L-1C与D溶液等体积混合,溶液呈酸性.
回答下列问题:
(1)D是______溶液
(2)用水稀释0.1mol?L-1B时,溶液中随着水量的增加而减小的是______(填写序号)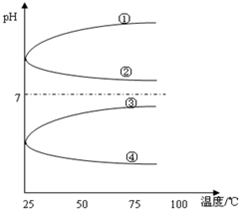
①
;②;
③c(H+)和c(OH-)的乘积④OH-的物质的量
(3)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如图中的______曲线(填写序号).
(4)OH-浓度相同的等体积的两份溶液A和E,分别和锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是______(填写序号)
①反应所需要的时间E>A
②开始反应时的速率A>E
③参加反应的锌的物质的量A=E
④反应过程的平均速率E>A
⑤A溶液里有锌剩余
⑥E溶液里有锌剩余
(5)室温下,向0.01mol?L-1C溶液中滴加0.01mol?L-1D溶液至中性得到的溶液中所有离子的物质的量浓度大小关系为______.
参考答案:(1)中和酸性物质A只有NaOH、NH3?H2O,物质的量的A与等物质的量浓度B和D混合呈中性,D的用量少,说明D碱性比B的碱性强,所以D是NaOH,故答案为:NaOH;
(2)①、由NH3?H2O?OH-+NH4+可知,加水促进电离,则n(NH3?H2O)减少,n(OH-)增大,则C(NH3?H2O)C(OH-)=n(NH3?H2O)n(OH-)减小,故①错误;
②、由NH3?H2O?OH-+NH4+可知,加水促进电离,则n(NH3?H2O)减少,n(OH-)增大,c(NH3?H2O)、c(OH-)都减小,c(H+)减小,则c(OH-)c(H+)减小,故②正确;
③、因加水稀释时,温度不变,则c(H+)和c(OH-)的乘积不变,故③错误;
④、由NH3?H2O?OH-+NH4+可知,加水促进电离,OH-的物质的量增大,故④错误;
故答案为:①②;
(3)等体积、等物质的量浓度NH3?H2O和与NH4HSO4混合后溶液发生反应:NH3?H2O+NH4HSO4=(NH4)2SO4+H2O,NH4)2SO4要发生水NH4++H2O?NH3?H2O+H+,溶液呈酸性,加热水解平衡正向移动,c(H+)增大,pH减小,故答案为:④;
(4)①根据酸能与锌反应得到氢气,随着反应的进行,CH3COOH不断电离出H+,反应速率比盐酸中快,产生的氢气一样多,反应所需要的时间HCl>CH3COOH,故①错误;
②根据酸能与锌反应得到氢气,开始溶液中c(H+)相等,反应时的速率HCl=CH3COOH,故②错误;
③根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故③正确;
④根据酸能与锌反应得到氢气,随着反应的进行,CH3COOH不断电离出H+,反应速率比盐酸中快,故④正确;
⑤根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故⑤正确;
⑥根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故⑥错误;
故答案为:③④⑤;
(5)NH4HSO4中滴入NaOH溶液,NaOH首先与NH4HSO4电离出的H+作用,因为H+结合OH-的能力比NH4+结合OH-的能量强(原因是产物H2O比NH3?H2O更难电离).当加入等摩尔的NaOH时,正好将H+中和,此时c(Na+)=c(SO42-),但此时溶液中还有NH4+,NH4+水解使溶液呈酸性,因此要使溶液呈中性,则还需继续滴入NaOH,当然到中性时c(OH-)=c(H+),c(Na+)>c(SO42- )>c(NH4+),故答案为:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
本题解析:
本题难度:简单
3、选择题 下列说法正确的是
[? ]
A.在漂白粉中滴入70%的硫酸,立刻产生黄绿色气体,说明硫酸具有还原性
B.粗锌与稀硫酸反应比纯锌快,说明粗锌反应时形成了原电池
C.硬水含有Ca2+、Mg2+、HCO3-、SO42-,煮沸可以完全除去其中的Ca2+、Mg2+
D.pH相同的两种一元酸HA溶液和HB溶液与足量Zn反应,HA比HB反应速率快,说明HA酸性更强
参考答案:B
本题解析:
本题难度:一般
4、填空题 下列说法是否正确?为什么?
(1)NH3在碱性溶液中比在纯水的溶解度大。
??
(2)氯化钠和醋酸铵的pH都接近于7,因此它们都没有发生水解。
?
参考答案:(1)不正确。NH3溶于水,存在溶解平衡、化学平衡和电离平衡:
NH3 (g) NH3 (aq);NH3 + H2O
NH3 (aq);NH3 + H2O NH3・H2O
NH3・H2O NH4+ + OH-
NH4+ + OH-
碱性溶液中c (OH-)较大,会促使上述平衡逆向移动,使得NH3的溶解度下降。
(2)不正确。氯化钠pH接近于7,是因为Na+、Cl-不影响水的电离;没有发生水解。而醋酸铵的pH接近于7,是因为CH3COO-、NH4+都发生了水解,只是水解程度几乎相同。
本题解析:(1)不正确,因为NH3溶于水,存在溶解平衡、化学平衡和电离平衡:
NH3 (g) NH3 (aq);NH3 + H2O
NH3 (aq);NH3 + H2O NH3・H2O
NH3・H2O NH4+ + OH-
NH4+ + OH-
碱性溶液中c (OH-)较大,会促使上述平衡逆向移动,使得NH3的溶解度下降。
(2)不正确,氯化钠pH接近于7,是因为Na+、Cl-不影响水的电离;没有发生水解。而醋酸铵的pH接近于7,是因为CH3COO-、NH4+都发生了水解,但二者的水解程度几乎相同,所以溶液显中性。
本题难度:一般
5、简答题 已知某溶液中只存在OH-、H+、Na+、CH3COO-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
②c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
③c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
④c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
填写下列空白:
(1)若溶液中溶解了一种溶质,则该溶质是______,则该溶液中四种离子浓度的大小顺序符合上述4种关系中的______.(填序号)
(2)若上述关系①是正确的,则溶液中的溶质为______;若上述关系②是正确的,则溶液中的溶质为______.
(3)若该溶液是由体积相等的NaOH溶液和醋酸混合而成,且恰好呈中性,则混合前c(NaOH)______c(CH3COOH)(填“大于”、“小于”、或“等于”,下同),混合后溶液中C(CH3COO-)______C(Na+).
参考答案:①溶液呈酸性,醋酸过量;
②溶液呈碱性,c(OH-)>c(CH3COO-),应为CH3COONa与NaOH的混合物;
③溶液呈碱性,可能为CH3COONa溶液,也可能为CH3COONa与CH3COOH的混合物;
④溶液呈酸性,醋酸过量,c(H+)>c(Na+),说明所加入NaOH很少.
(1)若溶液中溶解了一种溶质,则该溶质是只能是CH3COONa,则该溶液中四种离子浓度的大小顺序
c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故答案为:CH3COONa;③;
(2)若上述关系①是正确的,溶液呈酸性,醋酸过量溶液中的溶质为CH3COONa与CH3COOH的混合物,若上述关系②是正确的,溶液呈碱性,c(OH-)>c(CH3COO-),应为CH3COONa与NaOH的混合物,
故答案为:CH3COONa与CH3COOH;CH3COONa与NaOH;
(3)若该溶液是由体积相等的NaOH溶液和醋酸混合而成,且恰好呈中性,则溶液中c(H+)=c(OH-),根据溶液呈电中性,则C(CH3COO-)=c(Na+),由于醋酸为弱酸,
则混合前c(CH3COOH)>c(NaOH),故答案为:小于;等于.
本题解析:
本题难度:一般