1、选择题 把一定量的NaHCO3和Na2O2的混合物放在密闭容器中加热.关于混合物加热前后消耗盐酸的物质的量,下列判断正确的是
[? ]
A.加热前消耗的多
B.加热后消耗的多
C.加热前和加热后消耗的一样多
D.不知NaHCO3和Na2O2的含量无法确定
参考答案:C
本题解析:
本题难度:简单
2、简答题 碳酸钠(Na2CO3)和碳酸氢钠(NaHCO3)都可作为食用碱.
(1)用如图装置分别加热上述两种固体,当观察到澄清石灰水变浑浊时,则试管中加热的固体是______.
(2)若分别向碳酸钠溶液和碳酸氢钠溶液中滴加足量稀盐酸,都能观察到的现象是______,其中碳酸氢钠和稀盐酸反应的化学方程式为______.
(3)钠的化合物中,除了碳酸钠和碳酸氢钠外,还有______、______等.
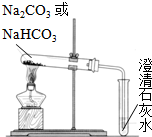
参考答案:(1)NaHCO3受热易分解,Na2CO3受热不分解,则观察到澄清石灰水变浑浊时,则试管中加热的固体是NaHCO3,故答案为:NaHCO3;
(2)二者均与盐酸反应生成二氧化碳,观察到的现象为有气泡冒出,碳酸氢钠与盐酸反应生成氯化钠、水、二氧化碳,其化学反应为NaHCO3+HCl=NaCl+H2O+CO2↑,
故答案为:有气泡冒出;NaHCO3+HCl=NaCl+H2O+CO2↑;
(3)氧化钠、氯化钠、过氧化钠、硫酸钠等均为常见的钠的化合物,故答案为:氧化钠;氯化钠.
本题解析:
本题难度:一般
3、选择题 有关Na2CO3和NaHCO3的性质,下列叙述中错误的是?
[? ]
A.将等浓度的Na2CO3溶液和NaHCO3溶液混合,向其中逐滴加入稀盐酸,首先发生HCO3-+H+===CO2↑+H2O
B.常温时水溶性:Na2CO3>NaHCO3
C.在酒精灯加热的条件下,前者不分解,后者分解
D.将澄清的石灰水分别加入Na2CO3和NaHCO3溶液中,均产生沉淀.
参考答案:A
本题解析:
本题难度:简单
4、简答题 下列四种鉴别无水碳酸钠和碳酸氢钠的方法是否可行?可行的写出实验现象及结论,不可行的说明理由
(1)2支试管中分别放入约1g的两种试样,分别滴入10滴水______.
(2)将试样配成物质的量浓度相同的溶液,分别滴入数滴酚酞______.
(3)2支试管中分别放入约1g的两种试样,分别加热______.
(4)2支试管中分别放入约1g的两种试样,分别加入足量的稀盐酸______.
参考答案:(1)相同条件下,碳酸钠的溶解度大,则方案可行,现象为粉末粘结且放热的是Na2CO3,粉末部分成溶液的为NaHCO3,
故答案为:可行,粉末粘结且放热的是Na2CO3,粉末部分成溶液的为NaHCO3;
(2)水解显碱性,等浓度时碳酸钠水解程度大,则方案可行,现象为溶液的红色较深的是Na2CO3,较浅的为NaHCO3,
故答案为:可行,溶液的红色较深的是Na2CO3,较浅的为NaHCO3;
(3)因碳酸氢钠受热易分解,而碳酸钠不分解,则方案可行,现象为试管壁有水珠的是NaHCO3,无明显变化的为Na2CO3,
故答案为:可行,试管壁有水珠的是NaHCO3,无明显变化的为Na2CO3;
(4)因碳酸钠、碳酸氢钠与盐酸反应聚生成气体,且产生气体的速率的差别甚小,难以作出正确判断,所以方案不可行,
故答案为:不可行,都有气体产生且产生气体的速率的差别甚小,难以作出正确判断.
本题解析:
本题难度:简单
5、选择题 下列实验“操作和现象”与“结论”对应关系正确的是( )
| 操作和现象 | 结论
A
向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体
HNO3分解成了NO2
B
向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成
淀粉没有水解成葡萄糖
C
向无水乙醇中加入浓H2SO4,加热至170℃,产生的气体通入酸性KMnO4溶液,紫红色褪去
使溶液褪色的气体是乙烯
D
向饱和Na2CO3溶液中通入足量CO2,溶液变浑浊
析出了NaHCO3
|
A.A
B.B
C.C
D.D
参考答案:D
本题解析:
本题难度:一般