1、简答题 化合物KxFe(C2O4)y-zH2O(Fe为+3价)是一种光敏感材料,实验室可以用如下方法制备这种材料并测定其组成.
I.制备:

(1)结晶时应将饱和溶液在黑暗处等待晶体的析出,这样操作的原因是______.
(2)操作Ⅲ的名称是______.
Ⅱ.组成测定:
称取0.491g实验所得晶体(假设是纯净物)置于锥形瓶中,加足量蒸馏水和稀H2SO4.将C2O42-完全转化为H2C2O4,用0.10mol-L-1KMnO4溶液进行滴定,消耗KMnO4溶液12.00mL时恰好反应;再加入适量的还原剂,将Fe3+完全转化为Fe2+,用KMnO4溶液继续滴定,当Fe2+完全氧化时,用去KMnO4溶液2.00mL.相关反应如下:
2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
(3)配制250mL?0.10mol-L-1KMnO4溶液及上述滴定实验中所需的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒、锥形瓶外还有______和______.两个滴定中到达终点时溶液颜色为______色,且30秒内不变色.
(4)通过计算,求此光敏材料的化学式______.
2、简答题 标况下充满HCl的烧瓶做完喷泉实验后得到稀盐酸,用标准碳酸钠溶液滴定这种盐酸测定它的准确浓度,请你回答下列问题:
(1)用标准碳酸钠溶液滴定这种盐酸时,碳酸钠溶液应装在______式滴定管中,若用甲基橙作指示剂,达到滴定终点时,溶液从______色变成______色.
(2)现配制三种浓度的标准碳酸钠溶液,你认为最合适的是下列第______种.
①2.500mol/L?②0.25mol/L?③0.025mol/L
(3)若采用上述合适的标准碳酸钠溶液滴定,用c(Na2CO3)表示,滴定时实验数据列表如下:
| 实验次数编号 | 待测盐酸体积(mL) | 滴入碳酸钠溶液体积(mL)
1
20.00
18.80
2
20.00
16.95
3
20.00
17.05
|
求这种待测稀盐酸的物质的量浓度(用题中所给数据列出计算式即可).c(HCl)=______.
(4)若盛装Na2CO3溶液的滴定管在滴定前未用标准液润洗,则最后所测盐酸浓度______,若滴定完毕后读数时俯视,则实验误差为______(以上两空填“偏高”、“偏低”或“无影响”)
来源:91考试网 91EXAm.org 3、选择题 下列实验方法或操作正确的是( )
A.酸碱中和滴定时,右手旋转滴定管的活塞,左手摇动锥型瓶,眼睛注视滴定管中的液面
B.用200mL烧杯配制物质的量浓度约为0.1000mol/L氢氧化钠溶液200mL
C.不用另加任何试剂就能鉴别NaAlO2、Na2SiO3、HCl、NaCl四种无色溶液
D.用托盘天平称取1.6g硫酸铜晶体配制100mL?0.1mol/L的硫酸铜溶液
4、选择题 下列有关实验原理或实验操作结论正确的是
[? ]
A.?配制酸性KMnO4溶液时,用盐酸酸化
B.?用水湿润pH试纸测量某溶液的pH值
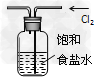
C.?实验室用上图所示装置除去Cl2中的少量HCl
D.?用盐酸标准溶液滴定待测的氢氧化钠溶液时,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低
5、选择题 实验室现有3种指示剂,其pH变色范围如下:甲基橙:3.1~4.4;?石蕊:5.0~8.0;?酚酞:8.2~10.0.用0.1000mol/L?NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述中正确定是( )
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,可选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,可选用酚酞作指示剂