1、选择题 在标准状况下体积最小的是
A.0.4molNO2
B.4gO2
C.1.505×1023个H2分子
D.11.2LCH4
参考答案:B
本题解析:分析:标准状况下Vm=22.4L/mol,根据n= =
= =
= ,先计算出物质的物质的量,气体的物质的量越多,则体积越大.
,先计算出物质的物质的量,气体的物质的量越多,则体积越大.
解答:已知:
A.n(NO2)=0.4mol;
B.n(O2)=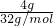 =0.125mol;
=0.125mol;
C.n(H2)=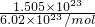 =0.25mol;
=0.25mol;
D.n(CH4)= =0.5mol,
=0.5mol,
则4gO2的物质的量最少,体积最小,
故选B.
点评:本题考查物质的量的相关计算,题目难度不大,本题注意相关计算公式的运用.
本题难度:简单
2、选择题 NA表示阿伏加德罗常数。下列说法正确的是
[? ]
A.7.8 g Na2O2中含有的阴离子数目为0.2NA
B.标准状况下,2. 24 L CHCl3的分子数为0.1NA
C.1 L 0.1mol/LAl2(SO4)3溶液中Al3+的数目为0.2NA
D.9.2 g NO2和N2O4的混合气中含有的氮原子数为0. 2NA
参考答案:D
本题解析:
本题难度:简单
3、简答题 下列对阿伏加德罗常数的理解,正确的是( )
A.阿伏加德罗常数是化学上常用的一个单位
B.某物质含有8mol分子,也可以说该物质含有的分子数目为8NA
C.通常情况下,近似值6.02×1023就是我们所说的阿伏加德罗常数
D.粒子数目越多,所含粒子的物质的量不一定越大
参考答案:A、阿伏加德罗常数是一个物理量,其单位是/mol,故A错误;
B、1mol分子含有的分子数目就是NA个分子,常用近似值6.02×1023个分子来表示,所以某物质含有8mol分子,也可以说该物质含有的分子数目为8NA,故B正确;
C、阿伏加德罗常数是有单位的,通常情况下,近似值6.02×1023/mol就是我们所说的阿状加德罗常数,故C错误;
D、根据n=NNA分析,粒子的数目越多,所含该粒子的物质的量一定越大,故D错误.
故选B.
本题解析:
本题难度:一般
4、选择题 用NA表示阿佛加德罗常数,下列说法中正确的是( )
A.Na2O2与H2O反应生成2.24LO2,反应中转移的电子数为0.2NA
B.4.5gSiO2晶体中含有的硅氧键数目为0.3NA
C.标准状况下,11.2L的SO3所含分子数为0.5NA
D.18g重水(D2O)所含的电子数为10NA
参考答案:A、若为标准状况下,2.24LO2的物质的量为0.1mol,氧气为氧化产物,反应中转移的电子数为0.1mol×2×NAmol-1=0.2NA,但氧气所处不一定是标准状况,2.24LO2的物质的量不一定为0.1mol,使用转移电子数不一定为0.2NA,故A错误;
B、4.5gSiO2晶体的物质的量为4.5g60g/mol=0.075mol,每摩尔二氧化硅含有4mol硅氧键,所以4.5gSiO2晶体含有硅氧键数目为0.075mol×4×NAmol-1=0.3NA,故B正确;
C、标准状况下,SO3是固体,不能使用气体摩尔体积22.4L/mol,故C错误;
D、18g重水(D2O)的物质的量为18g20g/mol=0.9mol,每个重水(D2O)分子含有10个电子,18g重水(D2O)含有的电子数为0.9mol×10×NAmol-1=9NA,故D错误.
故选:B.
本题解析:
本题难度:一般
5、选择题 用NA表示阿伏加德罗常数的值,下列关于0.3mol/L的MgCl2溶液的说法中,正确的是
[? ]
A.?100mL的溶液中含有Mg2+ 、Cl-的总数为0.3NA
B.?100mL的溶液中含有Mg2+的数目是0.1NA
C.?1L溶液中Mg2+的浓度是0.3mol/L
D.?1.5L溶液中含有Cl-的浓度是4.5mol/L
参考答案:C
本题解析:
本题难度:简单