1、选择题 某小组为研究电化学原理,设计如图装置,下列叙述不正确的是
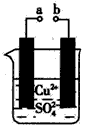
[? ]
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为Cu2++2e-=Cu
C.无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色
D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
参考答案:D
本题解析:
本题难度:一般
2、推断题 镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、炭粉、氧化铁等涂覆在铝箔上制成.由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收研究,并设计出相关实验流程图
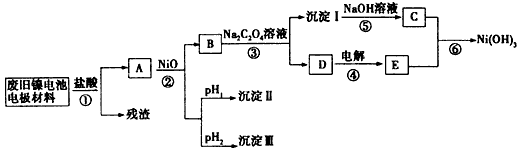
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如表所示:

回答下列问题:
(1)根据表数据判断步骤②依次析出沉淀Ⅱ 和沉淀Ⅲ (填化学式),则pH1 pH2(填填“>”、“=”或“<”),控制两种沉淀析出可利用 。
A.pH试纸 B.石蕊指示剂 C.pH计
(2)已知溶解度:NiC2O4>NiC2O4?H2O>NiC2O4?2H2O,则反应③的化学方程式是 。第③步反应后,过滤沉淀时需要的玻璃仪器有 。若过滤时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因 、 。
(3)④中阳极反应产生的气体E为 ,验证该气体的试剂为 。
(4)试写出反应⑥的离子方程式 。
参考答案:(1)Fe(OH)3 Al(OH)3 < C
(2)NiCl2+Na2C2O4+2H2O=NiC2O4・2H2O+2NaCl ;烧杯、漏斗、玻璃棒;滤纸破损、过滤液的液面高于滤纸的边缘
(3)Cl2;湿润的淀粉碘化钾试纸
(4)2Ni(OH)2+Cl2+2OH―=2Ni(OH)3+2Cl―
本题解析:由题给条件,金属氢氧化物的Ksp及沉淀析出的理论pH,可知,在A溶液中加入NiO是为了调节溶液pH,使相应的铝离子、三价铁离子全部沉淀出,Ni2+在溶液B中.根据pH可以确定开始析出沉淀和全部沉淀的pH范围,先析出沉淀Ⅱ是Fe(OH)3,沉淀pH范围是2.53~2.94,然后析出沉淀Ⅲ是Al(OH)3,沉淀PH的范围3.43~4.19,所以pH1<pH2;控制两种沉淀析出必须准确测定pH值,所以应利用pH计测定。
(2)由溶解度:NiC2O4>NiC2O4?H2O>NiC2O4?2H2O,结合流程中的变化
可知沉淀为溶解度小的NiC2O4?2H2O,所以根据转化关系写出化学方程式;
在过滤装置中用到的玻璃仪器和注意问题,根据装置和操作步骤写出NiCl2+Na2C2O4+2H2O=NiC2O4・2H2O+2NaCl,漏斗,烧杯、玻璃棒;滤纸破损、过滤液的液面高于滤纸的边缘。
(3)由流程图和以上分析可知,D溶液主要是氯化钠溶液,电解氯化钠溶液在阳极得到氯气,阴极得到氢气,所以E气体是Clc 2,验证氯气的试剂应是淀粉碘化钾溶液,遇氯气变蓝;
(4)在B溶液中加入Na2C2O4溶液生成了沉淀ⅠNiC2O4.2H2O,沉淀中加入氢氧化钠溶液,根据Ni(OH)2开始沉淀到全部沉淀的pH范围为7.60~9.75,加入过量氢氧化钠溶液能使沉淀NiC2O4・2H2O转化为Ni(OH)2,所以C为沉淀Ni(OH)2;根据流程图中的转化关系,沉淀C和氯气能生成Ni(OH)3,镍元素化合价升高是被氯气氧化的结果,因此离子方程式为2Ni(OH)2+2OH-+Cl2=2Ni(OH)3+2Cl-
本题难度:困难
3、填空题 (9分)下图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
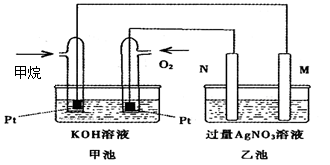
(1)N的电极反应式为 :
乙池的总化学方程式是 ,
加入甲烷的铂电极的电极反应式为 。
(2)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为 L(标准状况下);若此时乙池溶液的体积为200mL,则乙池中溶液的H+的浓度为 。
参考答案:(1)4OH--4e-=O2↑+2H2O(1分);
4AgNO3+2H2O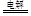 4Ag+4HNO3+2O2↑(2分);
4Ag+4HNO3+2O2↑(2分);
CH4-8e-+10OH-=CO32-+7H2O(2分)
(2)0.224(2分);0.2mol/L(2分)
本题解析:(1)甲池是以氢氧化钾溶液为电解液的甲烷燃料电池,通入甲烷的一极为原电池的负极,电极反应式为:CH4-8e-+10OH-=CO32-+7H2O,通入氧气的一极为原电池的正极,电极反应式为:O2 + 2H2O + 4e-=4OH-;乙池为电解池,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,N连接原电池的正极,为电解池的阳极,应为石墨材料,N为阳极,电极反应式是4OH--4e-=O2↑+2H2O,M为阴极,电极反应式为Ag++e-=Ag,电解的总反应为:4AgNO3+2H2O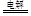 4Ag+4HNO3+2O2↑;(2)n(Ag)=0.04mol,根据Ag++e-=Ag可知转移电子为0.04mol,甲池中通入氧气的一极为正极,电极反应式为:O2 + 2H2O + 4e- = 4OH-,则消耗n(O2)=0.01mol,
4Ag+4HNO3+2O2↑;(2)n(Ag)=0.04mol,根据Ag++e-=Ag可知转移电子为0.04mol,甲池中通入氧气的一极为正极,电极反应式为:O2 + 2H2O + 4e- = 4OH-,则消耗n(O2)=0.01mol,
V(O2)=0.224L;根据反应4AgNO3+2H2O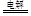 4Ag+4HNO3+2O2↑知,n(H+)=n(HNO3)=0.04mol,又溶液的体积为200mL,则c(H+)=0.2mol/L。
4Ag+4HNO3+2O2↑知,n(H+)=n(HNO3)=0.04mol,又溶液的体积为200mL,则c(H+)=0.2mol/L。
考点:考查原电池原理、燃料电池及电解原理的应用。
本题难度:困难
4、选择题 通以相等的电量,分别电解等浓度的硝酸银和硝酸亚汞(亚汞的化合价为+1)溶液,若被还原的硝酸银和硝酸亚汞的物质的量之比n(硝酸银) ∶n(硝酸亚汞)=2∶1,则下列叙述正确的是
[? ]
A.在两个阴极上得到的银和汞的物质的量之比n(银) ∶n(汞)=2∶1
B.在两个阳极上得到的产物的物质的量不相等
C.硝酸亚汞的化学式为HgNO3
D.硝酸亚汞的化学式为Hg2(NO3)2
参考答案:D
本题解析:
本题难度:一般
5、选择题 关于下图所示各装置的叙述中,正确的是

[? ]
A.装置①是原电池,总反应是:Cu + 2Fe3+ = Cu2+ + 2Fe2+
B.装置①中,铁做负极,电极反应式为:Fe3+ + e- = Fe2+
C.装置②通电一段时间后石墨Ⅱ电极附近溶液红褐色加深
D.若用装置③精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液
参考答案:C
本题解析:
本题难度:一般