1、填空题 下图各物质是中学化学中常见的物质,甲、乙均是离子化合物,且阴、阳离子个数比为1∶1。甲可作发酵粉,乙是一种常用的化肥。B、D常温下是气体。请回答下列问题:
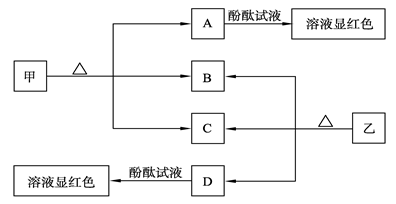
(1)甲的俗名是____________。
(2)D的水溶液滴入酚酞试液后,溶液显红色,请用必要的文字加以解释并写出相关的离子方程式:___?_________。
(3)甲溶液中加入氯化铝溶液,可以观察到的现象为?试写出反应的离子方程式:____?
参考答案:(1)小苏打(1分)
(2)D为NH3,溶于水后形成NH3.H2O为弱碱NH3 + H2O = NH3.H2O = NH4+ + OH-(3分,文字说明1分,方程式2分,只写氨水电离得1分)
(3)有白色沉淀生成同时有大量气泡产生(2分);3HCO3-+Al3+=Al(OH)3↓ +3CO2↑(2分)
本题解析:下图各物质是中学化学中常见的物质,甲、乙均是离子化合物,且阴、阳离子个数比为1∶1。甲可作发酵粉,可知甲为碳酸氢钠,A是碳酸钠,B是二氧化碳,C是水。乙是一种常用的化肥。B、D常温下是气体。则D为氨气。乙为碳酸氢铵。则)甲的俗名是小苏打。(2)D为NH3,溶于水后形成NH3.H2O为弱碱NH3 + H2O = NH3.H2O = NH4+ + OH-(3)甲溶液中加入氯化铝溶液,发生了双水解反应,可以观察到的现象为有白色沉淀生成同时有大量气泡产生离子方程式:3HCO3-+Al3+=Al(OH)3↓ +3CO2↑。
本题难度:一般
2、填空题 (10分)下图中的每一个方格表示有关的一种反应物或生成物,其中A,C,D为无色气体.请填下列空白: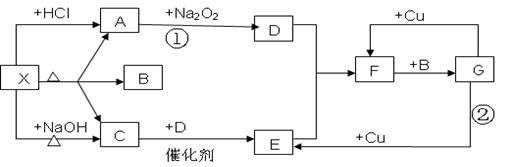
(1)物质X可以是______________________,C 是____________,F是____________.
(2)反应①化学方程式是________________________________________________。
(3)反应②的离子方程式是______________________________________________。
参考答案:(10分)
(1)? (NH4)2CO3?或NH4HCO3,?NH3 ,? NO2
(2 )? 2CO2+2Na2O2=2Na2CO3+O2
(3 )? 2NO3- + 8 H+ + 3Cu==2NO+3Cu2++4H2O
H+ + 3Cu==2NO+3Cu2++4H2O
本题解析:略
本题难度:一般
3、填空题 (10分)已知:①A、B、C、D四种物质均含有元素X,有的还有可能含有元素Y、Z。且元素Y、X、Z的原子序数依次递增。②X在A、B、C、D四种物质中都不呈现其最高化合价。③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。④化合物D受热分解,可制得元素Y的单质。试根据以上叙述回答:
(1)写出A、B、C、D的化学式::A_______B_______C_______D______。
(2)写出③、④中的两个化学方程式:
③,?④ ?。
参考答案:Cl2? KCl? KClO? KClO3
本题解析:由题意可知,X元素具有多种价态(至少4种),可得X元素一定为非金属元素,在非金属元素单质中能与某种常见一元强碱溶液反应的物质为CL2,即X元素为CL元素。化合物D受热分解,又含CL元素,所以为KCLO3,即B和C必为KCL和KCLO中的一种,综上所述:A:CL2? B与C为KCL或KCLO? D:KCLO3
③CL2+2NaOH=NaCL+NaCLO+H2O;④2KCLO3=====2KCL + 3O2↑
本题难度:一般
4、填空题 (7分)下图所表示的是中学化学中一类常见的物质转化关系(反应生成的H2O均略去),试按要求回答问题:
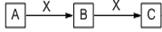
(1)若A为空气中含量最多的单质,C为一种红棕色的气体,则B与X的反应方程式为?
(2)若A为有臭鸡蛋气味的气体,C为H2SO3的酸酐,则B为:?,1molA与a molX充分燃烧,若要求既生成B又生成C,则a的取值范围为?
参考答案:(1)2NO+O2= 2NO2(2分)
(2)S(或硫)(2分)? 0.5<a<1.5(3分)
本题解析:略
本题难度:一般
5、推断题 A、B、C、D是由前18号元素组成的四种常见化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如下反应关系
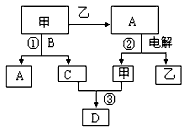
(1)上述转化过程中包含的反应类型为____________。
a.置换反应 b.化合反应 c.分解反应 d.复分解反应
(2)乙在甲中燃烧,当有1 mol e-转移,生成液态A时,放出 142.9 kJ的热量,写出该反应的热化学方程式:_____________________。
(3)反应③在一定条件下为可逆反应,经过一段时间该反应达到平衡,写出该反应的化学方程式:
____________________。若将3 mol甲和4 mol C混合充入容积为2 L的密闭容器中,2分钟后,达到平衡。平衡后混合气总物质的量为6 mol,甲的化学反应速率为____________。将该平衡混和物缓慢通入水中得到1L溶液,所得溶液物质的量浓度是____________。
参考答案:(1)bc
(2)H2(g) + 1/2O2(g) = H2O(l) △H=-285.8 kJ/mol
(3)2NO + O2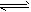 2NO2;0.25 mol/(L・min);4mol/L
2NO2;0.25 mol/(L・min);4mol/L
本题解析:
本题难度:一般