1��ѡ���� ��������5��˵����
�ٽ�������ǵ�Ӿ��ǰ��������
�������ʳ���ǻ����������
�����ᡢ�ռ�������ηֱ�Ϊ�ᡢ��Σ�
�ܹŴ�����ͭ����Խ�����������Ⱦ��ǺϽ�
����Һ��������ȷ�ɢϵ��
���д�����ǣ�������
A���٢ڢ�
B���٢ڢۢܢ�
C���ۢ�
D���ڢ�
�ο��𰸣��ٽ��岻���磬�������磬���Խ��������ǵ�Ӿ��ǰ���������ʢٴ���
����ĸ���������������ȫ����H+�Ļ��������ᣮ
�������Ȼ����ˮ��Һ���ǻ������ǻ����ʳ���������ˮ��Һ��Ҳ�ǻ������ǻ������˵�����ʳ���ǻ������������Dz���ȷ�ģ��ʡ����ڴ���
����������ռ����������ƣ��Ǽ������̼���ƣ����Σ��ʢ���ȷ��
�ܹŴ�����ͭ����Խ�����������Ⱦ��ǺϽ𣮹ʢ���ȷ��
�ݷ�ɢϵ��Ϊ��Һ�����塢��Һ���ʢݴ���
�ʴ�����Т٢ڢݣ�
��ѡA��
���������
�����Ѷȣ�һ��
2��ѡ���� ij����ѧϰС�����۱������ٽ�����ͨ������������Һ�ɵõ�Ư��Һ�ڿ�ͨ��ʯ�ͷ���õ����顢��ϩ�ͱ��۲���ֺ�Ŀǰ��ͨ��Ӳ�Ҷ��ǺϽ�?�����ᡢ��������ƺ���ʯ�ҷֱ������ᡢ��κ�������?��ú��ʯ�Ͷ��ǿ�������Դ������˵����ȷ���ǣ�������
A���٢ڢ�
B���٢�
C���ڢ�
D���ۢ�
�ο��𰸣��ٳ����£�������ͨ������������Һ�п��Եõ��Դ�������Ϊ��Ч�ɷֵ�Ư��Һ���仯ѧ����ʽΪ��Cl2+2NaOH�TNaCl+NaClO+H2O���ʢ���ȷ��
��ʯ�͵ķ����ܵõ����顢��ϩ�ȣ�ֻ�ܵĵ����͡�ú�͡����͵������ͺ����ͣ�Ȼ���������پ����ѽ���Եõ����顢��ϩ��С��������ͨ��ú�ĸ���ɵõ������ʢڴ���
�۲����Ϊ���Ͻ�1��Ӳ��Ϊ����֣�5�ǵ�Ϊ��о��ͭ��1Ԫ��Ϊ��о���������ǺϽ𣬹ʢ���ȷ��
������������������ȫΪ�����ӣ�����������������Ӻ�̼���������ɣ������Σ��������������Ӻʹ����������������Σ���ʯ���ɸƺ�������Ԫ����ɵĻ��������������ʢܴ���
����̫���ܡ����ܡ�ˮ���Լ�����ֲ���������Գ����ṩ�������������Դ���ڿ�������Դ������ú��ʯ�͡���Ȼ�����˿����ʯ�������Դ��һ�����ľͺ�����������Դ���Dz���������Դ���ʢݴ���
��ѡB��
���������
�����Ѷȣ�һ��
3��ѡ���� ���и����ʣ������ʡ�����������˳�����е��ǣ�?��
A��Һ̬�����ռ���
B����ʯ�ҡ����ס���ʯ��
C���ɱ��������Ȼ���
D������������������
�ο��𰸣�A
���������A����ȷ
B����ʯ��Ϊ���������Ϊ���ʣ���ʯ��Ϊ������
C���ɱ�Ϊ�������Ϊ���ʣ��Ȼ���Ϊ������
D������Ϊ��������Ϊ���ʡ�����Ϊ������
��ΪA
�����Ѷȣ���
4��ѡ���� ��ϡ���ᡢ����ռС�մ�����������������һ����̼��������̼�����ۡ���Ƭ��ľ̿��11�������У�ѡ���ʵ�������ȷ����ͼ�е�5�����ʣ�ʹ���ߵ����������ܷ�����Ӧ��
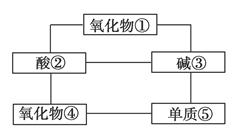
(1)д�����ǵĻ�ѧʽ��
��________����________����________����________����________��
(2)д����������뵥�ʢݷ�Ӧ�Ļ�ѧ����ʽ_____________________________________
�ο��𰸣�(1)��Al2O3����H2SO4����NaOH����Fe2O3����Al
(2)2Al��Fe2O3 Al2O3��2Fe
Al2O3��2Fe
���������������ΪAl2O3��Fe2O3��CO��CO2����ΪH2SO4����ΪNaOH������ΪAl��Fe��C������ΪNa2CO3���ռ�ΪNaOH��С�մ�ΪNaHCO3��������ټ����ᷴӦ������Ӧ��˵����������Ϊ����������ʢ�ΪAl2O3�����ʢ���Ӧ��˵����ΪAl������������ᷴӦ�����뵥�ʢݷ�Ӧ��˵���������ΪFe2O3������Al��Ӧ�Ļ�ѧ����ʽΪ2Al��Fe2O3 Al2O3��2Fe��
Al2O3��2Fe��
�����Ѷȣ�һ��
5��ѡ���� ����˵����ȷ����? (����)
A��������Һ���ܵ����H���Ļ����ﶼ������
B����ˮ��Ӧ��������������һ���Ǹ��������
C�����������������������
D�����ܸ��ᷴӦ��������һ������Ӧ
�ο��𰸣�B
���������A. ������Һ���ܵ����������ȫΪH���Ļ����ﶼ������
C�����������������������
D�����ܸ��ᷴӦ��������Ҳ��һ������Ӧ���粻���������һ����̼��
�����Ѷȣ���