1、选择题 将0.lmol・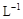 醋酸溶液加水稀释,下列说法正确的是()
醋酸溶液加水稀释,下列说法正确的是()
A.溶液中c(H+)和c(OH-)都减小
B.溶液中c(H+)增大
C.醋酸电离平衡向左移动
D.溶液的pH增大
参考答案:D
本题解析:醋酸溶液加水稀释,促进醋酸电离,C错误;n(H+)增大,c(H+)减小,c(OH-)增大,pH增大,A、B错误,D正确。
点评:酸溶液加水稀释,c(H+)减小,c(OH-)增大。
本题难度:一般
2、选择题 下列说法正确的是( )
A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4
B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸
C.用0.2000mol/L?NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1mol/L),至中性时,溶液中的酸未被完全中和
D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1mol/L盐酸、③0.1mol/L氯化镁溶液、④0.1mol/L硝酸银溶液中,Ag+浓度:①>④=②>③
参考答案:A、稀释醋酸时能促进弱电解质醋酸的电离,导致稀释后溶液中氢离子浓度大于原来的110,稀释后溶液的3<pH<4,故A错误;
B、NaHA溶液的pH>7说明H2A的二级电离,不完全电离,即HA-为弱酸,可以说明H2A是弱酸,NaHA溶液的pH<7,H2A是强酸或弱酸都有可能,如硫酸、亚硫酸,故B错误;
C、NaOH滴定HCl与CH3COOH,醋酸是弱电解质,若碱与酸恰好反应,溶液中溶质为氯化钠、醋酸钠,醋酸根水解溶液呈碱性,反应呈中性,溶液中的酸有剩余,故C正确;
D、氯化银难溶于水,在水中的溶解度很小,一定温度下,溶液中Ksp(AgCl)=c(Ag+)?c(Cl-)为定值,①蒸馏水中没有氯离子、②0.1mol/L盐酸中c(Cl-)=0.1mol/L,③0.1?mol/L氯化镁溶液c(Cl-)=0.2mol/L、④0.1mol/L硝酸银溶液中c(Ag+)=0.1mol/L,溶液中c(Ag+)为④>①>②>③,故D错误.
故选:C.
本题解析:
本题难度:一般
3、选择题 将0.1mol?L-1氨水溶液加水稀释或加入少量NH4Cl晶体时,都会引起( )
A.溶液的pH减小
B.NH3?H2O电离程度变大
C.溶液的导电能力减弱
D.溶液中c(H+)减小
参考答案:A.加水稀释氨水,促进一水合氨电离,但氢氧根离子浓度增加的量远远小于溶液体积增加的量,所以氢氧根离子浓度减小,溶液的pH减小;向氨水中加入少量氯化铵晶体,铵根离子浓度增大抑制一水合氨电离,则溶液中氢氧根离子浓度减小,溶液的pH减小,故A正确;
B.加水稀释氨水,促进一水合氨电离,向氨水中加入氯化铵晶体,铵根离子浓度增大,抑制一水合氨电离,故B错误;
C.加水稀释氨水,促进一水合氨电离,但氢氧根离子浓度增加的量远远小于溶液体积增加的量,所以氢氧根离子浓度减小,溶液的导电能力减弱;向氨水中加入氯化铵,溶液中离子浓度增大,导电能力增强,故C错误;
D.无论稀释氨水还是加入氯化铵晶体,溶液中氢氧根离子浓度都减小,温度不变,水的离子积常数不变,则氢离子浓度增大,故D错误;
故选:A.
本题解析:
本题难度:一般
4、选择题 相同物质的量浓度的下列物质的稀溶液中,pH最小的是( )
A.乙醇
B.乙酸
C.碳酸钠
D.碳酸
参考答案:B
本题解析:
本题难度:简单
5、选择题 某温度下,可逆反应HA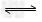 H++A-的电离常数为Ka,下列说法正确的是
H++A-的电离常数为Ka,下列说法正确的是
[? ]
A.Ka越大,表示该弱酸较易电离
B.Ka越大,表示该弱酸较难电离
C.Ka随反应物浓度的改变而改变
D.Ka随体系温度的改变而改变
参考答案:AD
本题解析:
本题难度:一般