1、选择题 要检验某溴乙烷中的溴元素,正确的实验方法是( )
A.加入溴水振荡,观察水层是否有棕红色出现
B.滴入AgNO3溶液,再加入稀硝酸呈酸性,观察有无浅黄色沉淀生成
C.加入NaOH溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,观察有无浅黄色沉淀生成
D.加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成
参考答案:检验溴乙烷中含有溴元素首先将它转化为溴离子,采用卤代烃的水解方法,即加入氢氧化钠,在水解后生成的溴离子可以和银离子反应,生成淡黄色不溶于硝酸的沉淀溴化银,由此来检验溴乙烷中的溴元素,所以操作为:加入NaOH溶液,加热,溴乙烷在碱性条件下水解生成溴化钠和乙醇,冷却,加入稀HNO3酸化后加入AgNO3溶液,溴离子和银离子反应生成淡黄色不溶于硝酸的溴化银沉淀.
故选C.
本题解析:
本题难度:简单
2、计算题 某一氯代烷1.85 g,与足量的NaOH水溶液混合加热后,用硝酸酸化,再加入足量AgNO3溶液,生成白色沉淀2.87 g。
(1)通过计算,写出这种一氯代烷的各种同分异构体的结构简式。
(2)若此一氯代烷与足量NaOH溶液共热后,不经硝酸酸化就加AgNO3溶液,将会产生什么现象?写出有关化学反应方程式。
(3)能否用硝酸银溶液直接与卤代烷反应来鉴别卤代烷?为什么?
参考答案:(1)同分异构体的可能结构有:
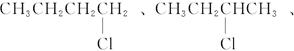
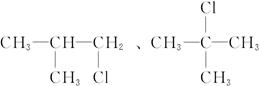
(2)若C4H9Cl与NaOH水溶液共热后不经硝酸酸化就加AgNO3溶液,将会产生褐色沉淀。因为过量的NaOH能与AgNO3反应,生成白色的AgOH沉淀,AgOH不稳定,立即分解为褐色Ag2O。有关的化学方程式为:
AgNO3+NaOH====AgOH↓+NaNO3
2AgOH====Ag2O+H2O
(3)不能用硝酸银溶液直接与卤代烃反应来鉴别卤代烃。因为卤代烃中的卤素均是以卤原子的形式与碳原子结合,不能在水溶液中直接电离出X-(F-、Cl-、Br-、I-),故不能与Ag+反应产生沉淀。
本题解析:(1)一氯代烷的通式为CnH2n+1Cl,有关反应的方程式为:
CnH2n+1Cl+H2O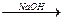 CnH2n+1OH+HCl
CnH2n+1OH+HCl
HCl+NaOH====NaCl+H2O
NaOH+HNO3====NaNO3+H2O
NaCl+AgNO3====AgCl↓+NaNO3
则1 mol CnH2n+1Cl相当于1 mol AgCl,即:
CnH2n+1Cl?―? AgCl
14n+36.5? 143.5
1.85 g? 2.87 g
 ?n=4
?n=4
因此,一氯代烷的分子式为C4H9Cl,其同分异构体的可能结构有:
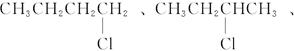
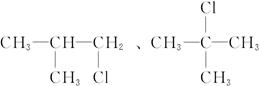
(2)若C4H9Cl与NaOH水溶液共热后不经硝酸酸化就加AgNO3溶液,将会产生褐色沉淀。因为过量的NaOH能与AgNO3反应,生成白色的AgOH沉淀,AgOH不稳定,立即分解为褐色Ag2O。有关的化学方程式为:
AgNO3+NaOH====AgOH↓+NaNO3
2AgOH====Ag2O+H2O
(3)不能用硝酸银溶液直接与卤代烃反应来鉴别卤代烃。因为卤代烃中的卤素均是以卤原子的形式与碳原子结合,不能在水溶液中直接电离出X-(F-、Cl-、Br-、I-),故不能与Ag+反应产生沉淀。
本题难度:简单
3、选择题 化合物Z由如下反应得到: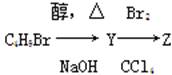 ,Z的结构简式不可能是( )
,Z的结构简式不可能是( )
A.CH3CH2CHBrCH2Br
B.CH3CH(CH2Br)2
C.CH3CHBrCHBrCH3
D.CH2BrCBr(CH3)2
参考答案:B
本题解析:由反应流程知:Y必为烯烃,Z为两个溴原子在相邻碳原子上的卤代烃,故B错;A、C、D均可能。
本题难度:一般
4、选择题 如图表示4―溴环己烯所发生的4个不同反应。其中,产物只含有一种官能团的反应是
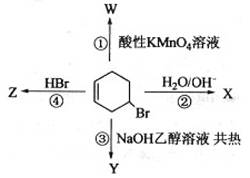
A.①④
B.③④
C.②③
D.①②
参考答案:B
本题解析:由结构可知,有机物中含C=C和-Br,①为氧化反应,得到两种官能团;②为水解反应,得到C=C和-OH两种官能团;③为消去反应,产物中只有C=C;④为加成反应,产物中只有-Br,则有机产物只含有一种官能团的反应是③④,故选B.
本题难度:一般
5、选择题 下列卤代烃在KOH醇溶液中加热不反应的是

[? ]
A. ①②⑥
B. ①⑤⑥
C. ①③⑥
D. ③④⑥
参考答案:C
本题解析:
本题难度:一般