1、选择题 已知可逆反应2SO2+O2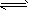 2SO3,当生成2molSO3时放出热量为Q,现将1mol SO2和0.5mol O2在相同条件下反应生成SO3放出的热量为Q1,则
2SO3,当生成2molSO3时放出热量为Q,现将1mol SO2和0.5mol O2在相同条件下反应生成SO3放出的热量为Q1,则
[? ]
A.Q1=1/2Q
B.Q1<1/2Q
C.2Q1>Q
D.无法判断
参考答案:B
本题解析:
本题难度:一般
2、填空题 以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表。
难溶物
| Ksp
|
Ca3(AsO4)2
| 6.8× 10-19 10-19
|
AlAsO4
| 1.6×1 0-16 0-16
|
FeAsO4
| 5.7×10-21
|
污染物
| H2SO4
| As
|
浓度
| 28.42 g/L
| 1.6 g・L-1
|
排放标准
| pH 6~9
| 0.5 mg・L-1
|
表1.几种砷酸盐的Ksp?表2.工厂污染物排放浓度及允许排放标准
回答以下问题:
⑴该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=? ▲?mol・L-1。
⑵写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]=? ▲?,若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol・L-1,c(AsO43-)的最大是? ▲?mol・L-1。
⑶工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式? ▲?。
⑷在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为? ▲?;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为? ▲?。
参考答案:
⑴0.29
⑵c3 (Ca2+)・c2 (AsO43-)? 5.7×10-17
⑶2H++MnO2+H3AsO3=H3AsO4+Mn2++H2O
⑷①CaSO4?②H3AsO4是弱酸,当溶液中pH调节到8左右时AsO43-浓度增大,Ca3(AsO4)2开始沉淀
本题解析:
略
本题难度:简单
3、填空题 某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如右图所示。由图中数据分析,该反应的化学方程式为_______?_______________________。
反应开始至2min,Z的平均反应速率为____?________________。
参考答案:X+3Y  2Z? 0.05 mol/(L・min)
2Z? 0.05 mol/(L・min)
本题解析:根据图像可知,反应进行到2min时物质的浓度不再发生变化,此时X和Y的物质的量分别减少了1.0mol-0.9mol=0.1mol和1.0mol-0.7mol=0.3mol,Z的物质的量增加了0.2mol。所以根据变化量之比是相应的化学计量数之比可知,反应的方程式是X+3Y  2Z。此时Z的平均反应速率是
2Z。此时Z的平均反应速率是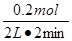 =0.05 mol/(L・min)。
=0.05 mol/(L・min)。
点评:该题是高考中的常见题型,属于基础性试题的考查。试题基础性强,侧重对学生基础知识的巩固和训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确物质的变化量之比和化学计量数之比的关系,然后灵活运用即可。
本题难度:一般
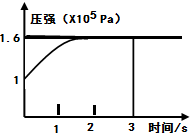
4、选择题 一定温度下,向体积为2L的恒容密闭容器中充入1mol PCl5(g),发生反应:PCl5(g) PCl3(g)+Cl2(g)?△H=+Q? KJ/mol维持容器温度不变,测得容器内压强随反应时间的变化如图所示。下列说法正确的是(?)
PCl3(g)+Cl2(g)?△H=+Q? KJ/mol维持容器温度不变,测得容器内压强随反应时间的变化如图所示。下列说法正确的是(?)
A.3s内的平均速率为:V(PCl3)=0.1mol・L-1・min-1
B.达到平衡时放出0.6QKJ热量
C.其他条件不变,再向容器中充入1molPCl5(g),则达新平衡 时,C(PCl5)>0.4mol・L-1
D.其他条件不变,增大PCl5的浓度,平衡常数减小
参考答案:C
本题解析: A.恒温、恒容的密闭容器中,气体的物质的量之比等于压强之比,则平衡时混合气体的物质的量为1.6mol,气体的物质的量增大(1.6-1)mol=0.6mol,设生成PCl3的物质的量为x,
PCl5(g)?PCl3(g)+Cl2(g) 气体增加的物质的量
1mol? 1mol
x? 0.6mol
x=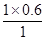 mol=0.6mol,
mol=0.6mol,
V(PCl3)==0.1mol/(L.s),时间单位是S不是min,错误;B.该反应是吸热反应不是放热反应,当气体增加1mol时吸收的热量是QKJ,则气体增加0.6mol时吸收的热量是0.6QKJ,错误;? C.平衡体系中再加入1mol的PCl5,重新到达平衡状态,可以等效为开始加入2mol的PCl5,体积增大为原来的2倍,达平衡(该平衡与原平衡等效)后再将体积压缩到原来大小,与原平衡相比,压强增大,平衡向逆反应方向移动,则平衡浓度大于原来的两倍,正确;D.温度不变,平衡常数不变,错误.
本题难度:一般
5、填空题 在0.5 L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
ΔH<0,其化学平衡常数K与温度T的关系如下表:
?
请完成下列问题:
(1)试比较K1、K2的大小,K1________K2(填“>”“=”或“<”)
(2)下列各项能作为判断该反应达到化学平衡状态的依据的是________(填字母编号)
a.容器内N2、H2、NH3的浓度之比为1∶3∶2
b.v正(N2)=3v逆(H2)
c.容器内压强保持不变
d.混合气体的密度保持不变
(3)400 ℃时,反应2NH3(g) N2(g)+3H2(g)的化学平衡常数K的值为________,当测得NH3和N2、H2的物质的量分别为3 mol和2 mol、1 mol时,该反应的v正(N2)________v逆(N2)(填“>”“<”或“=”)
N2(g)+3H2(g)的化学平衡常数K的值为________,当测得NH3和N2、H2的物质的量分别为3 mol和2 mol、1 mol时,该反应的v正(N2)________v逆(N2)(填“>”“<”或“=”)
参考答案:(1)> (2)c (3)2 >
本题解析:(1)因反应是放热反应,升温平衡向左移动,反应程度减小,故K1>K2;(2)因反应前后气体总体积发生变化,故压强不变,说明反应混合物中各组分的含量不变,即反应处于平衡状态;反应前后气体质量不变,容器容积不变,故反应过程中混合气体的密度一直保持不变;反应平衡时,3v正(N2)=v逆(H2);容器中N2、H2、NH3的浓度之比与反应是否达到平衡状态无关;(3)在400℃时,合成氨反应N2(g)+3H2(g) 2NH3(g)的化学平衡常数K=0.5,故400℃时,2NH3(g)
2NH3(g)的化学平衡常数K=0.5,故400℃时,2NH3(g) N2(g)+3H2(g)的化学平衡常数为
N2(g)+3H2(g)的化学平衡常数为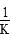 =2;利用容器中各物质的物质的量浓度可知:Q=
=2;利用容器中各物质的物质的量浓度可知:Q=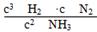 =
=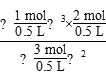 =
= <2,所以反应2 NH3(g)
<2,所以反应2 NH3(g) N2(g)+3H2(g)向右进行,v正(N2)>v逆(N2)
N2(g)+3H2(g)向右进行,v正(N2)>v逆(N2)
本题难度:一般