1、填空题 (10分)甲、乙两池电极材料如图所示,请按要求回答下列问题:
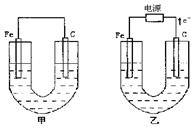
(1)若两池中均为Cu(NO3)2溶液,反应一段时间后:①有红色物质析出的是甲池中的____ 棒(铁、碳);
②乙池碳极上电极反应属于___________(填氧化反应、还原反应)。
③乙池中阳极上发生的电极反应方程式是 _________________。
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的化学方程式 。
②甲池中碳极上电极反应方程式是 。
③若乙池中饱和NaCl溶液100 mL一段时间后在阴极得到112 mL(标准状况)H2,此时乙池溶液的(体积变化忽略不计)pH为__________
(3)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:①阳电极的材料是____________
②阴极反应式是 。(说明:杂质发生的电极反应不必写出)
参考答案:(10分(1))①碳 ;②氧化反应 ③4OH-―4e-====O2↑+2H2O
(2)①2H2O+2NaCl====2NaOH+H2↑+Cl2↑
②O2 + 4e-+ 2H2O 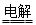 4OH-,③、13
4OH-,③、13
(3)①粗铜 ②Cu2+ +2e-="===" Cu
本题解析:略
本题难度:一般
2、填空题 (14分)铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料。
(1)铝元素在元素周期表中的位置是____ 。
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。
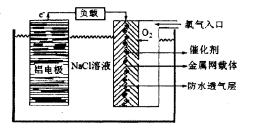
①该电池的总反应化学方程式为____ ;
②电池中NaCI的作用是 。
③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料)时,电解过程中阳极的电极反应式为 。
④某铝一空气电池的效率为50%,若用其作电源电解500mL的饱和NaCI溶液,电解结束后,所得溶液(假设溶液电解前后体积不变)中NaOH的浓度为0.3 mol・L-1,则该过程中消耗铝的质量为 。(3)氯化铝广泛用于有机合成和石油工业的催化剂,聚氯化铝也被用于城市污水处理。
①氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则其结构式为 。
②将铝土矿粉与碳粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式 。
参考答案:20、(1)第三周期第ⅢA族;(2)①4Al+3O2+6H2O=4Al(OH)3 ②增强溶液的导电能力;
③I-+3H2O-6e-=IO3-+6H+ ④2.7g (3) ①
②Al2O3+3C+3Cl2 2AlCl3+3CO.
2AlCl3+3CO.
本题解析:(1)铝原子原子核外有3个电子层,最外层上有3个电子,所以其在周期表中的位置是第三周期第ⅢA族,答案为:第三周期第ⅢA族;(2)①铝和氧气、水能反应生成氢氧化铝,反应方程式为:4Al+3O2+6H2O=4Al(OH)3,答案为:4Al+3O2+6H2O=4Al(OH)3;②溶液中自由移动的离子浓度越大,溶液的导电性越强,水是弱电解质导电能力较小,为增大水的导电性,所以加入氯化钠,答案为:增强溶液的导电能力;③阳极上失电子发生氧化反应,所以电解碘化钾溶液时,阳极上碘离子放电和水反应生成碘酸根离子和氢离子,电极反应式为:I-+3H2O-6e-=IO3-+6H+,答案为:I-+3H2O-6e-=IO3-+6H+;
④电解氯化钠溶液后,氢氧化钠的物质的量=0.3mol/L×0.5L=0.15mol,设电解过程中电子转移的物质的量是x,
2NaCl+2H2O 2NaOH+Cl2↑+H2↑ 转移电子
2NaOH+Cl2↑+H2↑ 转移电子
2mol 2mol
0.15mol x x=0.15mol
某铝一空气电池的效率为50%,所以原电池中转移电子的物质的量是0.3mol,设消耗铝的质量为y.
Al- 3e- =Al3+
27g 3mol
y 0.3mol y=2.7g 答案为:2.7g;
(3)①氯化铝为共价化合物,氯原子提供孤对对子,铝原子提供空轨道,形成配位键,使所有原子均达到8电子稳定结构,所以结构式为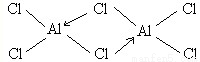 ;
;
②根据题意知,反应物是氧化铝、碳和氯气,反应条件是加热,生成物是氯化铝和一氧化碳,所以其反应方程式为:Al2O3+3C+3Cl2 2AlCl3+3CO,答案为:Al2O3+3C+3Cl2
2AlCl3+3CO,答案为:Al2O3+3C+3Cl2 2AlCl3+3CO.
2AlCl3+3CO.
考点:考查铝及其化合物的性质。
本题难度:困难
3、选择题 汽车的启动电源常用铅蓄电池,放电时其电池反应如下:PbO2+Pb+2H2SO4="=" 2PbSO4+2H2O。根据此反应判断,下列叙述中正确的是
A.Pb是正极
B.PbO2得电子,被氧化
C.负极反应是Pb+SO42――2e―="=" PbSO4
D.电池放电时,溶液酸性增强