1、选择题 在Na2S水溶液中c(Na+)与c(S2-)的关系是
[? ]
A.c(Na+)=2c(S2-)
B.c(Na+)<2c(S2-)
C.c(Na+)>2c(S2-)
D.2c(Na+)=c(S2-)
参考答案:C
本题解析:
本题难度:一般
2、选择题 下列叙述正确的是
A.CO2水溶液的导电性较弱,故CO2属于弱电解质
B.BaSO4难溶于水,属于非电解质
C.强电解质比弱电解质的水溶液导电能力强
D.向较浓的醋酸溶液中逐滴加入浓氨水,导电实验显示,混合溶液的导电能力开始有一个由弱到强的变化过程
参考答案:D
本题解析:
本题难度:困难
3、选择题 氢氧化钡溶液中滴入等物质的量浓度的硫酸溶液并测定溶液导电性,下面各图表示的是随着硫酸滴入量的变化溶液导电能力变化的图象,其图象表示正确的是(横坐标为硫酸滴入量,纵坐标为导电性)( )
A.

B.
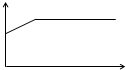
C.

D.
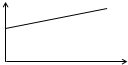
参考答案:A
本题解析:
本题难度:简单
4、选择题 下列叙述中正确的是
A.电解质在通电时才能发生电离
B.Fe可以导电,但它不是化合物,所以Fe不是电解质,而是非电解质
C.电解质并不一定导电,导电的物质不一定是电解质
D.某物质若不是电解质,就一定是非电解质
参考答案:C
本题解析:电解质在水分子作用下也能电离,选项A不正确;Fe为单质,电解质和非电解质是对化合物而言的,选项B不正确;单质和混合物既不是电解质也不是非电解质,选项D不正确.
本题难度:简单
5、选择题 对下列物质:①H2SO4、②CO2、③NaOH、④BaSO4、⑤NH3、⑥SO2、⑦NH3?H2O、⑧C2H5OH、⑨Cu、⑩氯化钠溶液按要求分类不正确的是( )
A.弱电解质:④、⑦
B.电解质:①、③、④、⑦
C.非电解质:②、⑤、⑥、⑧
D.强电解质:①、③、④
参考答案::①H2SO4在水溶液里,能完全电离出自由移动的氢离子和硫酸根离子导致导电,所以H2SO4是强电解质;
②CO2在水溶液里,生成碳酸,碳酸能电离出自由移动的氢离子和碳酸根离子导致导电,不是二氧化碳自身电离,所以二氧化碳是非电解质;
③NaOH在水溶液里或在熔融状态下,能完全电离出自由移动的钠离子和氢氧根离子导致导电,所以NaOH是强电解质;
④BaSO4属于盐,溶于水的部分或者熔融状态时,可以完全电离变成离子,属于强电解质;
⑤NH3溶于水后,能和水反应生成一水合氨,一水合氨能电离出自由移动的阴阳离子,但电离出阴阳离子的是一水合氨,不是NH3,所以NH3是非电解质;
⑥SO2为化合物,其水溶液能导电,但其本身不发生电离,则属于非电解质;
⑦NH3?H2O在水溶液中不能完全电离,NH3?H2O是弱碱,是弱电解质;
⑧C2H5OH在水溶液中是以乙醇分子的形式存在,所以不导电,故它为非电解质;
⑨Cu能导电,是单质,它既不是电解质,也不是非电解质;
⑩氯化钠溶液能电离出自由移动的钠离子和氯离子,能导电,但它是混合物,它既不是电解质,也不是非电解质;
A.④BaSO4属于强电解质,⑦NH3?H2O是弱电解质,故A错误;
B.①H2SO4③NaOH、④BaSO4⑦NH3?H2O是电解质,故B正确;
C.②CO2⑤NH3、⑥SO2⑧C2H5OH是非电解质,故C正确;
D.①H2SO4③NaOH④BaSO4是强电解质,故D正确;
故选A.
本题解析:
本题难度:一般