1、实验题 (1)用简单的实验证明在氨水中存在NH3・H2O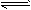 NH4++OH-的电离平衡(要求写出简单操作、现象及实验能说明的问题)。 _________________________________。
NH4++OH-的电离平衡(要求写出简单操作、现象及实验能说明的问题)。 _________________________________。
(2)老师给某学生提供下列药品和必要的实验仪器,要求学生设计实验证明醋酸是弱酸。药品为冰醋酸、蒸馏水和pH试纸。此同学思考后认为:
①设计的理论依据是_______________________________________;
②实验的简要步骤是_______________________________________;
③需记录的现象和数据是__________________________________;
④推断与分析:由于___________________________,说明________________,所以醋酸是弱酸。
参考答案:(1)在氨水中滴入酚酞试液变红,加入醋酸铵固体,振荡,溶液颜色明显变浅,说明c(OH-)减小,是
c(NH4+)增大平衡左移而造成的,由此证明氨水中存在着电离平衡
(2)①弱电解质稀释10a倍,pH改变小于a
②将一定浓度的醋酸稀释到一定量(如100倍)后,测量稀释前后溶液的pH
③稀释的倍数、稀释前后溶液的pH
④溶液稀释100倍后,溶液的pH改变小于2;稀释过程中醋酸的电离程度增大
本题解析:
本题难度:一般
2、实验题 为了探究铜与浓硫酸的反应,某研究性学习小组做了如下实验
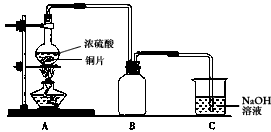
①在放有铜片的圆底烧瓶中加入10mL浓硫酸,加热煮沸10min(如图所示)后,所得固体分离除去未反应的铜片,再经水洗仍有大量黑色不溶物。
②取少量不溶物,向其中加入几滴浓硝酸,产生大量红棕色气体。
③取少量不溶物,向其中加5mL酒精,充分振荡后,静置、过滤,把滤液移入盛有水的小试管中,振荡,出现浑浊。
④取少量不溶物,向其中加入3mL氨水,振荡,溶液呈无色,在空气中静置,溶液变为深蓝色。
⑤取少量不溶物,向其中加入浓盐酸并加热,沉淀几乎全部溶解。为了解释上述现象,学习小组通过查阅资料了解到。
a.铜与浓硫酸反应的不溶性副产物可能有:CuS、Cu2S、Cu2O、S等物质;
b.CuS和Cu2S都能溶于热的浓盐酸;
c.Cu2O能溶于氨水生成无色的[Cu(NH3)2]+,[Cu(NH3)2]+在氨水中被空气中的氧气氧化成深蓝色的
[Cu(NH3)4]2+。
回答下列问题:
(1)实验结束后,装置C中的溶液中可能含有的溶质有__________________。
(2)第②步操作要注意的问题是_________________________;对比①②两步操作中的现象,你能得到的结论是_________________________。
(3)第③步操作中出现的沉淀是__________________,请解释出现这一现象的原因_______________。
(4)写出④步涉及的离子方程式______________________________。
(5)综合分析铜与浓硫酸的反应,生成的不溶物是___________________________。
(6)某工厂拟用废铜屑制备硫酸铜,请你分析利用上述实验原理是否可行。若可行,请说明理由____________________________________。若不可行,请设计更合理的实验方案(用化学反应方程式表示)
______________________________。
参考答案:(1)Na2SO3、NaOH、Na2SO4
(2)必须在密闭系统中(或在通风厨中)进行,防止污染空气(或防止中毒);黑色沉淀中有还原性物质,浓硝酸的氧化性强于浓硫酸。
(3)硫(或S);硫微溶于酒精但不溶于水,将硫的酒精溶液倒入水中,即可析出固体硫
(4)Cu2O+4NH3・H2O=2[Cu(NH3)2]++2OH-+3H2O,4[Cu(NH3)2]++8NH3・H2O+O2=4[Cu(NH3)4]2++4OH-+
6H2O
(5)Cu2O、S以及CuS和Cu2S中的一种或两种
(6)“略”
本题解析:
本题难度:困难
3、选择题 下列根据实验现象所作出的结论中一定正确的是
A.无色试液使红色石蕊试纸变蓝,结论:该试液一定是碱溶液
B.无色试液加入银氨溶液,加热出现银镜,结论:试液中含有醛类物质
C.无色试液焰色反应呈黄色,结论:试液中一定含有Na+
D.无色试液加入碳酸钠溶液产生白色沉淀,结论:试液中含氢氧化钙
参考答案:C
本题解析:略
本题难度:简单
4、实验题 某研究性学习小组在网上收集到如下信息:钾、钙、钠、镁等活泼金属都能在CO2气体中燃烧。他们对钠在CO2气体中燃烧后的产物中的白色物质进行了如下探究:
【实验】将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
(1)通过钠在CO2气体中燃烧的实验,你认为燃烧的条件是____________________。
(2)燃烧的本质是_______________________。
(3)2010年8月初发生的俄罗斯森林大火有比伦敦市还要大的面积。控制森林火灾是世界性难题。根据燃烧的条件,请你解释为什么设置森林防火隔离带能有效阻止森林火灾的蔓延?
__________________________________。
【提出假设】 假设1:白色物质是Na2O。 假设2:白色物质是Na2CO3。 假设3:白色物质是Na2O和
Na2CO3的混合物。
【设计实验方案.验证假设】该小组对燃烧后的白色产物进行如下探究:

【思考与交流】
(4)甲同学认为方案1得到的结论不正确,其理由是_______________________。
(5)乙同学认为方案2得到的结论正确,白色物质为_______________________。
(6)通过方案1和方案2的实验,你认为上述三个假设中,___________成立。你的理由是________________________________。
(7)钠在二氧化碳中燃烧的化学方程式为_________________________。
(8)丙同学认为白色物质有可能是氢氧化钠。你是否同意丙同学的观点,并简述理由:____________________________________。
参考答案:
(1)要有可燃物;要有助燃物;可燃物的温度必须达到着火点
(2)发光发热的剧烈的氧还反应
(3)消除了可燃物的存在
(4)Na2CO3显碱性,也会使酚酞变红
(5)Na2CO3
(6)假设2;方案2①中出现的白色沉淀说明有CO32-,②中加酚酞无明显现象说明无Na2O
(7)4Na+3CO2 2Na2CO3+C
2Na2CO3+C
(8)不同意,因为无氢元素(或其它合理答案)
本题解析:
本题难度:困难
5、实验题 在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
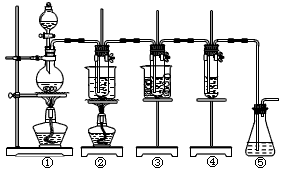
图中:
①为氯气发生装置;
②的试管里盛有15 mL 30% KOH溶液,并置于水浴中;
③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置。
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过_____________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_______(填写下列编号字母)的净化装置。
(A)碱石灰 (B)饱和食盐水 (C)浓硫酸 (D)饱和碳酸氢钠溶液
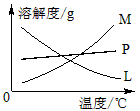
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是:___________________。反应完毕经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是_______(填写编号字母);从②的试管中分离出该晶体的方法是__________(填写实验操作名称)。
(3)本实验中制取次氯酸钠的离子方程式是________________________。
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白
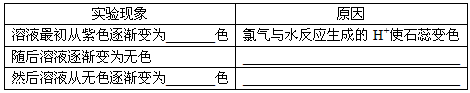
参考答案:(1)分液漏斗;B
(2)碱溶液(或反应物)的浓度不同,反应温度不同;M;过滤
(3)Cl2+2OH- = ClO-+Cl-+H2O(4)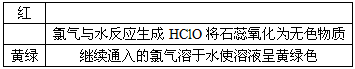
本题解析:
本题难度:一般