1������� ����ʧȥ��ǩ����ƿ��ɫ��ҺA��B��C��D��ֻ֪��������K2CO3��K2SO4��H2SO4��Ba��NO3��2��Ϊ�˼������ǣ���������ʵ�飺
��A+D-����Һ+���塡��B+C-����Һ+����
��B+D-����Һ+��������A+B-����Һ+����
�ݽ��ܵõ��ij���������������Һ�У����г����ܿ��ܽⲢ������ɫ��ζ����ζ��
��������ʵ����ʵ����ش��������⣺
��1��A��B��C��D������ɫ��Һ�ֱ�Ϊ______��______��______��______���û�ѧʽ��ʾ��
��2��д�����и�����Ӧ�����ӷ���ʽ
��______��______��______��
�ο��𰸣���1��B��A��C��D��϶��г���������BӦΪBa��NO3��2��A+D-����Һ+���壬ֻ��̼��غ����ᷴӦ���и����ڢۢܵõ��ij��������ᱵ������̼�ᱵ�����ܵõ��ij���������������Һ�У����г����ܿ��ܽⲢ������ɫ��ζ����ζ�����Ԣ��г���һ����̼�ᱵ������A��̼��أ�D�����ᣬC������أ�
�ʴ�Ϊ��H2SO4��Ba��NO3��2��K2SO4��K2CO3��
��2���ٵķ�Ӧʵ���ǣ�2H++CO32-=CO2��+H2O���ڵķ�Ӧʵ���ǣ�Ba2++SO42-=BaSO4�������ܵõ��ij�����̼�ᱵ�����������Һ�����У�
�ݵķ�Ӧʵ���ǣ�BaCO3+2H+=Ba2++CO2��+H2O���ʴ�Ϊ��2H++CO32-=CO2��+H2O��Ba2++SO42-=BaSO4����BaCO3+2H+=Ba2++CO2��+H2O��
���������
�����Ѷȣ�һ��
2��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ���ǣ�������
A���Ȼ�����Һ��ʴͭ�壺Fe3++Cu=Cu2++Fe2+
B����С�մ�����θ����ࣺHCO3-+H+=CO2��+H2O
C������ˮ��Ӧ��2Na+2H2O=2Na++2OH-+H2��
D����������Һ�еμӹ�����ˮ��Al3++4NH3?H2O=AlO2-+4NH4++2H2O
�ο��𰸣�A���Ȼ�����Һ��ʴͭ�壺2Fe3++Cu=Cu2++2Fe2+����A����
B����С�մ�����θ�����ķ�Ӧ���ӷ���ʽΪ��HCO3-+H+=CO2��+H2O����B��ȷ��
C������ˮ��Ӧ�����ӷ���ʽΪ��2Na+2H2O=2Na++2OH-+H2������C��ȷ��
D����������Һ�еμӹ�����ˮ��Al3++3NH3?H2O=Al��OH��3��+3NH4+����D����
��ѡBC��
���������
�����Ѷȣ�һ��
3��ѡ���� ����ȷ��ʾ���з�Ӧ�����ӷ���ʽΪ��?��
A����ϡ����ϴ���Թ��ڱڵ�������Ag��2H����NO3��=Ag����NO����H2O
B��������ϡ���BaS + 2H+ = H2S��+ Ba2+
C��0.01mol��L��1NH4Al(SO4)2��Һ��0.02mol��L��1Ba(OH)2��Һ�������ϣ�NH4��+Al3��+2SO42��+2Ba2��+4OH��=2BaSO4��+Al(OH)3��+NH3��H2O
D����NaHCO3��Һ�м�������ij���ʯ��ˮ�����ְ�ɫ����2HCO3-+Ca2++2OH-=CaCO3��+CO32-+2H2O
�ο��𰸣�C
���������A�������ӵ�ʧ���غ㣬B�������������ᱵ������C��ȷ��D����������̼��Ƴ������������ƺ�ˮ��
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ���ﲻ��ȷ����
A����SO2ˮ��Һ����Br2�� SO2 + Br2+2H2O =4H+ + SO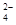 +2Br��
+2Br��
B����0.3mol/L���Ȼ����Һ��ȥ����������������������þ��Mg(OH)2 +2NH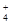 =Mg2++2NH3��H2O
=Mg2++2NH3��H2O
C�����Ը�����غ���������ȡ����������4MnO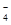 +4H2O2+12H+=4Mn2++7O2��+10H2O
+4H2O2+12H+=4Mn2++7O2��+10H2O
D���ö��Ե缫�������ͭ��Һ�� 2Cu2++ 2H2O  2Cu +O2�� +4H+
2Cu +O2�� +4H+
�ο��𰸣�C
���������
�𰸣�C
A����ȷ��SO2����������B����ȷ��Mg(OH)2�����OH�D��NH3��H2O���ã�C������ȷ��2MnO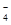 +5H2O2+6H+=2Mn2++8H2O��5O2����D����ȷ��Cu2�� ����������
+5H2O2+6H+=2Mn2++8H2O��5O2����D����ȷ��Cu2�� ����������
�����Ѷȣ�һ��
5��ѡ���� �������ӷ���ʽ��д��ȷ����
A��NaHSˮ�ⷴӦ��HS��+ H2O 
 H3O++ S2��
H3O++ S2��
B������������ˮ�������õ�ԭ��Al3++ 3H2O 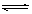 Al(OH)3(����) + 3H+
Al(OH)3(����) + 3H+
C������������Һ��ϡ���ᷴӦ��Ba2����SO 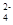 ��H����OH��===BaSO4����H2O
��H����OH��===BaSO4����H2O
D��̼��������Һ�м������Ba(OH)2��Һ��