1������� ����A��B��C��D��E��F��G���ֺ˵����С��18��Ԫ�أ����ǵ�ԭ������һ�ε��������У�Aԭ�Ӻ��������ӣ�Bԭ�������������Ǵ�����2����Dԭ������������������Ӳ�����3����Eԭ�Ӻ����һ��ȵ������������1��F���������������ڵ�һ���������G�γɵ�-1��������Arԭ�Ӻ�������Ų���ͬ��
�ɴ���֪��
��1��Aԭ�ӷ�����______��
��2��Bԭ�ӽṹʾ��ͼ��______
��3��GԪ���γɵĵ�����A��D��E��Ԫ���γɳʼ��ԵĻ����ﷴӦ�����ӷ���ʽ��______
����F�ֱ���C���ʡ�BDԪ���γɵĻ�������ȼ�յĻ�ѧ����ʽ��______��______��
�ο��𰸣�A��B��C��D��E��F��G���ֺ˵����С��18��Ԫ�أ����ǵ�ԭ���������ε��������У�Aԭ�Ӻ��������ӣ���A��HԪ�أ�Bԭ�������������Ǵ�����2������B��CԪ�أ�Dԭ������������������Ӳ�����3������D��OԪ�أ�C��ԭ����������BС��D������C��NԪ�أ�Eԭ�Ӻ����һ��ȵ������������1����E��NaԪ�أ�F���������������ڵ�һ�����������F��ԭ����������E������F��MgԪ�أ�G�γɵ�-1��������Arԭ�Ӻ�������Ų���ͬ����G��ClԪ�أ�
��1����AΪHԪ�أ���Aԭ�ӷ�����11H���ʴ�Ϊ��11H��
��2��BΪCԪ�أ�Cԭ�ӽṹʾ��ͼΪ
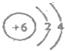
���ʴ�Ϊ��
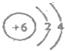
��
��3��GԪ���γɵĵ�����������A��D��E��Ԫ���γɳʼ��ԵĻ��������������ƣ�����������������Һ��Ӧ�����ӷ���ʽΪ��2OH-+Cl2�TCl-+ClO-+H2O��þ�ֱ��ڵ�����������̼��ȼ�յĻ�ѧ����ʽΪ��3Mg+N2?��ȼ?.?Mg3N2��2Mg+CO2?��ȼ?.?2MgO+C���ʴ�Ϊ��2OH-+Cl2�TCl-+ClO-+H2O��3Mg+N2?��ȼ?.?Mg3N2��2Mg+CO2?��ȼ?.?2MgO+C��
���������
�����Ѷȣ�һ��
2��ѡ���� ������Ԫ��A��B��C��D��ԭ���������ε��������ǵ�ԭ������֮��Ϊ34����ԭ�ӵ�����������֮��Ϊ10��A��C��ԭ������������֮�͵���Bԭ�ӵĴ�����������A��C��B��D��Ϊͬ����Ԫ�أ�����������ȷ���ǣ�������
A��B��D����������ﶼ���ܺ��κ��ᷴӦ
B������������Ӧˮ����ļ��ԣ�A��C
C��CΪͬ������ԭ�Ӱ뾶��С��Ԫ��
D������Ԫ�����γɻ���������������D
�ο��𰸣�A��Cͬ���壬A��Cԭ�ӵ�����������֮�͵���Bԭ�ӵĴ�������������A������������Ϊx����BΪ�ڶ�����Ԫ�أ���2x=2��x=1����AΪH��Li��ԭ������������֮��Ϊ10��B��Dͬ���壬����������ӦΪ4��ԭ���������ε��������ǵĺ˵����֮��Ϊ34����BΪC��CΪNa��DΪSi��AӦΪLi�����ǵĺ˵����3+6+11+14=34���������⣻��BΪ������Ԫ�أ���2x=8��x=4��AΪ̼��CΪ�裬A��B��C��Dԭ������֮�ʹ���34�����������⣬
A��DΪSi�����������ΪSiO2��SiO2����HF�ᷴӦ����A����
B�������ԣ�Na��Li��Ԫ�صĽ�����Խǿ����Ӧ������������Ӧˮ����ļ���Խǿ��������������Ӧˮ����ļ��ԣ�A��C����B��ȷ��
C��ͬ����Ԫ�ش�����Ԫ�ص�ԭ�Ӱ뾶��С����NaΪͬ������ԭ�Ӱ뾶����Ԫ�أ���C����
D��CԪ�����γ��л��������������࣬��D����
��ѡB��
���������
�����Ѷȣ�һ��
3������� A��B��C��D��E����Ԫ�أ����ǵ����������ε���������С��18��AԪ��ԭ�Ӻ���ֻ��1�����ӣ�BԪ��ԭ�Ӻ�CԪ��ԭ������������֮��Ϊ2��BԪ��ԭ��������ϵĵ�����Ϊ������������2����B��C��D����Ԫ�ؿ����γɻ�ѧʽΪD2BC3�Ļ��������ɫ��ӦΪ��ɫ��0.5mol?EԪ�صĵ������������ᷴӦ��9.03��1023�����ӷ���ת�ƣ���E��C�Ļ������У�E������ռ52.94%������֪E��ԭ�Ӻ�����14�����ӣ�
��1����������Ԫ�طֱ��ǣ�
A______��B______��C______��
��2������Dԭ�ӽṹʾ��ͼ��E�����ӽṹʾ��ͼ______��______��
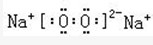
��3��д��A2C��BC2��D2C2�ĵ���ʽ______��______��______��
��4��д��D2C2��A2C��Ӧ�Ļ�ѧ����ʽ______��
�ο��𰸣���1��AԪ��ԭ�Ӻ���ֻ��1�����ӣ���AΪH��BԪ��ԭ��������ϵĵ�����Ϊ������������2������BΪC��BԪ��ԭ�Ӻ�CԪ��ԭ������������֮��Ϊ2�����������ε�������CΪO���ʴ�Ϊ����H�� ̼C����O��
��2��D2BC3�Ļ��������ɫ��ӦΪ��ɫ����DΪNa��0.5 mol EԪ�صĵ������������ᷴӦ��9.03��1023�����ӷ���ת�ƣ���EΪ+3�ۣ���E��C�Ļ�������E������ռ52.94%������֪E��ԭ�Ӻ�����14�����ӣ���EΪAl���ʴ�Ϊ��Na
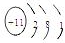
? Al3+
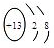
��
��3��A2CΪH2O��BC2ΪCO2��D2C2ΪNa2O2���ʴ�Ϊ��
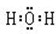
��
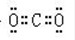
��
��
��4��D2C2��A2C��Ӧ�Ļ�ѧ����ʽ��2Na2O2+2H2O=4NaOH+O2�����ʴ�Ϊ2Na2O2+2H2O=4NaOH+O2����
���������
�����Ѷȣ�һ��
4��ѡ���� ����˵����ȷ���ǣ�������
A��Ԫ����������Ԫ��ԭ�Ӻ�������Ų������Ա仯�Ľ��
B��HCl��H2S��PH3��SiH4�����ȶ��Ժͻ�ԭ�Ծ�������ǿ
C���������ڷǽ���Ԫ�غ���������Դ�����������ǿ
D���ǽ���Ԫ�ص�ԭ����������γɵĻ����ﲻһ���ǹ��ۻ�����
�ο��𰸣�A
���������
�����Ѷȣ���
5��ѡ���� ij����Ԫ�ص�ԭ��,M������һ����������ܼ�,����ԭ�ӵ���������
[? ]
A��ֻ����7
B��ֻ����15
C����11��15
D����11��13
�ο��𰸣�C
���������
�����Ѷȣ���